EMA症例171:9月解説
2025年9月症例にご参加いただきました皆様,誠にありがとうございます.9月24日時点で質問に回答をいただいた方は 121 名いらっしゃいました.皆様の回答の集計結果を紹介します.
質問1:同居の母から追加で聴取したい項目を教えてください(自由回答,3つまで).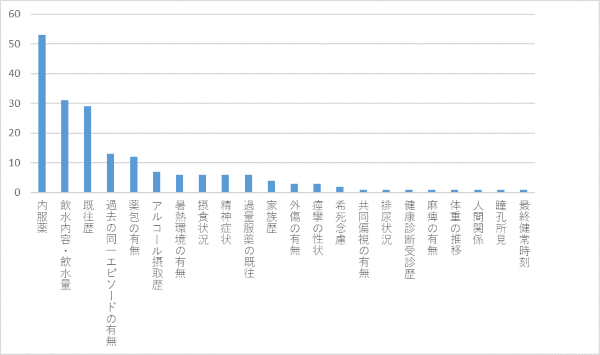
類似した回答はまとめさせていただいていますのでご了承ください.
内服薬が最多で,飲水エピソードがあったことからその内容や量についての質問が続きました.
既往歴に関しては甲状腺疾患や婦人科疾患といった具体的な疾患の有無を聴取したい旨の回答もありました.
質問2:意識障害の鑑別として,まず確認したい身体所見を教えてください(自由回答,1つ).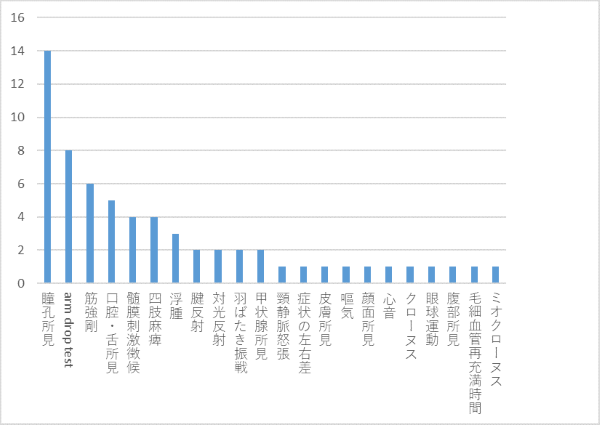
同様に類似した回答はまとめさせていただきました.
瞳孔所見を筆頭に神経学的所見が並び,浮腫や甲状腺といった回答もみられました.
質問3:あなたの診断は?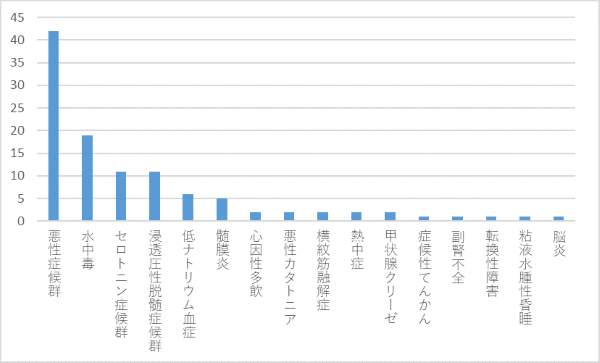
悪性症候群が最多であり,水中毒,セロトニン症候群,浸透圧性脱髄症候群と続きました.
質問4:あなたの属性は?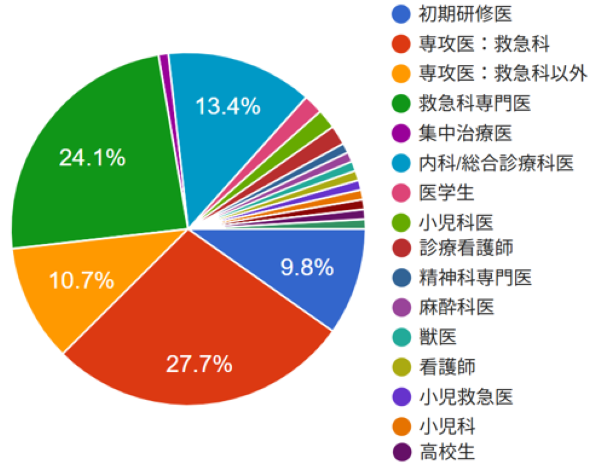
今回も多種多様な属性の方から回答いただきました.ありがとうございます.
まず,本症例のその後の経過です.
その後の症例の経過:
高体温,筋強剛,CPK上昇から悪性症候群と診断しました.原因として疑わしい薬剤はすべて中止し,気管挿管し人工呼吸管理を開始のうえ,深鎮静としウォーターパッドによる体温管理を実施しました.CPK値は順調に低下し,経時的な意識レベルの改善が得られました.入院8日目に抜管,入院13日目に自宅退院となりました.
解説:
本症例のテーマは,「悪性症候群」です.向精神薬の処方が増加している現代では救急外来でも遭遇する可能性が高く,意識障害の鑑別疾患として重要です.
■悪性症候群とは
悪性症候群は抗精神病薬の使用に関連して生じる神経救急疾患であり,特徴的な症状として意識障害,筋強剛,高体温,自律神経障害があります1).抗精神病薬を内服している患者の0.02-3%に発症するとされ2),若年成人に多く発症しますが年齢はリスク因子でなく,また性差もないとされています3).
ハロペリドールなど定型抗精神病薬での発症が多いとされていますが,リスペリドン,オランザピンといった非定型抗精神病薬での発症も報告されており,またメトクロプラミドやドンペリドンなどドパミンの関与する経路の阻害を機序にもつ制吐薬も原因薬となりえます3).これらの薬剤の開始もしくは増量から1週間以内での発症が大半を占めますが必ずしも短期間で発症するわけではなく,同じ薬を同じ用量で数年間使用していて発症した報告もあります4).抗精神病薬の高用量での使用,最近の増量,急激な増量,単剤から別の単剤への切り替え,非経口的投与がリスク因子として挙げられます5).
抗精神病薬に関連した発症に比して少数ですが,抗パーキンソン病薬の中止,減量,別薬剤への切り替えに関連した発症も報告されています.薬剤の中止などに加え感染,脱水,手術などの基礎因子の影響も受けます6).
またほかのリスク因子として,リチウム製剤やほか向精神薬の併用,強い薬効,徐放性製剤,薬物乱用,外傷や手術といった急性病態が挙げられます.
発症機序は明らかにはなっていませんが,ドパミン受容体の阻害が関連していると考えられています.視床下部でのドパミン受容体の阻害は高体温や自律神経障害を惹起し,黒質線条体を経由するドパミン経路の阻害ではパーキンソン症候群と同様の振戦や筋強剛が引き起こされるとされます7).また自律神経障害によって筋緊張が増し代謝も亢進し,場合により血圧や脈拍の不安定化も生じると考えられています.
一般的には2週間程度で症状の改善が得られるとされますが,徐放性製剤の使用やベースの中枢神経疾患があると罹病期間が延びることがあります.死亡例は5-10%とされますが,悪性症候群そのものよりも呼吸不全,敗血症,急性腎障害,心不全といった合併症によるものが多くを占めます.
■臨床的特徴と診断
前述の通り,典型的な症状として意識障害,筋強剛,高体温,自律神経障害があります.
意識障害は大半の患者の初期症状であり,妄想や幻覚よりも意識混濁を主とした低活動型せん妄様の症状が出現します.カタトニアや無言症も初期症状となり得ます.
筋強剛は全身にかつ高度に出現します.鉛管様抵抗であることが多いとされていますが,歯車様抵抗であることや振戦がみられることもあります.
高体温は多くの診断基準に含まれている重要項目であり,90%近くの症例で38℃以上となり,40℃以上のことも全症例の約40%と稀ではありません.ただ非定型抗精神病薬に関連した症例では認めないこともあります8).
自律神経障害は頻脈(88%)や血圧値不安定(61-77%),頻呼吸(73%)といった症状として現れることが多く,ほか不整脈や発汗過多も生じ得ます.
ほかジストニア,後弓反張,舞踏病,開口障害,構音障害,嚥下障害,唾液分泌過多といった症状も頻度は高くありませんが起きることがあります.
血液検査ではCPK上昇が典型的であり,100,000 IU/L以上まで上昇することもあります9).CPK上昇の程度は筋強剛の程度と関連するとされ,特に発症初期などで筋強剛が軽微である場合にはCPK上昇も軽微に留まることがあります.CPK値は重症度や予後とも相関があるとされます9).
そのほかの検査異常としては白血球増多,LDH上昇,ALP上昇,肝酵素上昇,代謝性アシドーシス,高ナトリウム血症,低ナトリウム血症,高カリウム血症,血清鉄低下といったものが挙げられますがいずれも特異的なものではありません.今回の症例では来院時点で低ナトリウム血症を認めていますが,多飲のエピソードもあったことから悪性症候群のみならず水中毒の要素もあったものと考えられます.入院翌日の血液検査で急激なナトリウム値の上昇がみられた点も,水中毒の要素を示唆します.浸透圧性脱髄症候群も鑑別となりますが,経時的に意識レベルの改善が得られた経過から否定的と考えます.
診断は上述の関連薬剤の投与歴と,典型的な症状との組み合わせで為されます.これまでに発表されている診断基準は複数あり,症状や検査異常のうちどの項目を含むかがそれぞれ異なっています10).2011年に国際的コンセンサスグループによって診断基準が発表され各項目に点数がつけられたスコアリングシステムとなっています(表1)11)が,診断のための閾値の設定はなく有用性の検証もなされていません.
表1:悪性症候群診断のためのスコアリングシステム
またこれまでに発表された診断基準のうち,頻用されるものにLevensonのものがあります(表2)12) .今回の症例では来院時点でMajor manifestationsのいずれも該当しませんが,入院後の経過ですべてを満たしたため診断に至りました.初診時には診断基準を満たさないこともあるため,疑わしい薬剤を内服している患者の意識障害では悪性症候群を念頭に置く必要があります
表2:Levensonの診断基準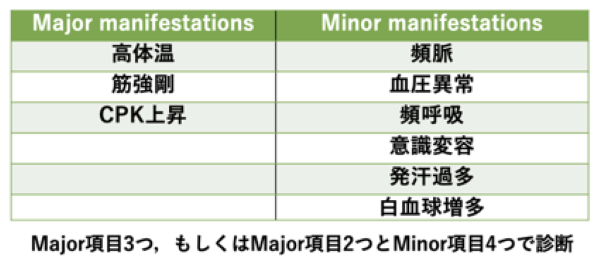
鑑別疾患として,セロトニン症候群,悪性高熱症,抗コリン作動性症候群,中枢神経感染症,敗血症,熱中症,アルコール離脱などが挙げられます.なかでもセロトニン症候群は薬剤に起因することなど類似点が多いですが,経過が早いこと,クローヌスがみられること,消化器症状が出現しやすいことといった特徴があります.EM Alliance教育班で過去に取り上げていますので,こちら(https://www.emalliance.org/education/case/kaisetsu8)もぜひご覧ください.
■治療
まず重要な治療としては原因と思われる薬剤の中止があります.リチウム製剤,抗コリン製剤,セロトニン受容体作動薬など症状に関連しうる薬剤も中止が望ましいです.
特に重症例では集中治療室でのモニタリングが必要となります.場合によって呼吸や循環のサポートとして人工呼吸管理や抗不整脈薬を使用します.気管挿管を要する場合にはサクシニルコリンでは不整脈や高カリウム血症を誘発しうるため,非脱分極性筋弛緩薬の使用が望まれます.また発汗や高体温で体液喪失が見込まれるため,適切な輸液管理が必要となります.CPK上昇が高度の場合には急性腎障害の予防のため大量輸液が行われることがありますが,尿のアルカリ化には強いエビデンスはありません.
高体温を改善させるためにクーリングブランケット,冷水による胃洗浄,腋窩クーリングなどのactive coolingを検討します.アセトアミノフェンも有用である可能性がありますがまだ確立された治療ではありません.
合併症として脱水,電解質異常,急性腎障害,不整脈,相対的心筋虚血,ストレス起因性心筋症,胸壁筋強剛による呼吸不全,敗血症,深部静脈血栓症などが生じることがあります.
ダントロレン,ブロモクリプチン,アマンタジンといった薬剤が使用されることがありますが,過去の症例報告や経験に基づくものであり確固たるエビデンスはないのが現状です.上記のような治療を行なっても改善が得られない場合や悪化の一途を辿る場合に使用が考慮されます.また同様に重症例では電気痙攣療法が行われることもあります.
いかがでしたでしょうか?
抗精神病薬を内服していて発症した悪性症候群の症例をご紹介しました.意識障害の触れ込みで搬送されると頭蓋内疾患に飛びついてしまいがちですが,それ以外の多数の鑑別疾患も忘れずに診療にあたってみてください.悪性症候群は問診(現病歴や既往歴,薬剤の使用について)とバイタルサイン,身体所見から診断に迫ることのできる疾患です.初診時には診断基準を満たさないこともあるため,向精神薬を内服している患者の意識障害では悪性症候群も念頭に置いて診療を進めましょう.改めて疾患の概要と治療について見直す一助となれましたら幸いです.
Take home message:
○病歴と身体所見から悪性症候群を診断しよう
○意識障害患者の対応では薬剤の関連した疾患を忘れないようにしよう
参考文献:
1) Wijdicks EFM, Ropper AH. Neuroleptic Malignant Syndrome. N Engl J Med. 2024 Sep 26;391(12):1130-1138. doi: 10.1056/NEJMra2404606. PMID: 39321364.
2) Velamoor VR. Neuroleptic malignant syndrome. Recognition, prevention and management. Drug Saf. 1998 Jul;19(1):73-82. doi: 10.2165/00002018-199819010-00006. PMID: 9673859.
3) Caroff SN, Mann SC. Neuroleptic malignant syndrome. Med Clin North Am. 1993 Jan;77(1):185-202. doi: 10.1016/s0025-7125(16)30278-4. PMID: 8093494.
4) Pope HG Jr, Aizley HG, Keck PE Jr, McElroy SL. Neuroleptic malignant syndrome: long-term follow-up of 20 cases. J Clin Psychiatry. 1991 May;52(5):208-12. PMID: 1674508.
5) Keck PE Jr, Pope HG Jr, Cohen BM, McElroy SL, Nierenberg AA. Risk factors for neuroleptic malignant syndrome. A case-control study. Arch Gen Psychiatry. 1989 Oct;46(10):914-8. doi: 10.1001/archpsyc.1989.01810100056011. PMID: 2572206.
6) Takubo H, Harada T, Hashimoto T, Inaba Y, Kanazawa I, Kuno S, Mizuno Y, Mizuta E, Murata M, Nagatsu T, Nakamura S, Yanagisawa N, Narabayashi H. A collaborative study on the malignant syndrome in Parkinson's disease and related disorders. Parkinsonism Relat Disord. 2003 Apr;9 Suppl 1:S31-41. doi: 10.1016/s1353-8020(02)00122-0. PMID: 12735913.
7) Henderson VW, Wooten GF. Neuroleptic malignant syndrome: a pathogenetic role for dopamine receptor blockade? Neurology. 1981 Feb;31(2):132-7. doi: 10.1212/wnl.31.2.132. PMID: 6110195.
8) Picard LS, Lindsay S, Strawn JR, Kaneria RM, Patel NC, Keck PE Jr. Atypical neuroleptic malignant syndrome: diagnostic controversies and considerations. Pharmacotherapy. 2008 Apr;28(4):530-5. doi: 10.1592/phco.28.4.530. PMID: 18363536.
9) Levenson JL. Neuroleptic malignant syndrome. Am J Psychiatry. 1985 Oct;142(10):1137-45. doi: 10.1176/ajp.142.10.1137. PMID: 2863986.
10) Sarkar S, Gupta N. Drug information update. Atypical antipsychotics and neuroleptic malignant syndrome: nuances and pragmatics of the association. BJPsych Bull. 2017 Aug;41(4):211-216. doi: 10.1192/pb.bp.116.053736. PMID: 28811916; PMCID: PMC5537576.
11) Gurrera RJ, Caroff SN, Cohen A, Carroll BT, DeRoos F, Francis A, Frucht S, Gupta S, Levenson JL, Mahmood A, Mann SC, Policastro MA, Rosebush PI, Rosenberg H, Sachdev PS, Trollor JN, Velamoor VR, Watson CB, Wilkinson JR. An international consensus study of neuroleptic malignant syndrome diagnostic criteria using the Delphi method. J Clin Psychiatry. 2011 Sep;72(9):1222-8. doi: 10.4088/JCP.10m06438. Epub 2011 Jun 28. PMID: 21733489.
12) Pandya M, Pozuelo L. A malignant neuroleptic spectrum: review of diagnostic criteria and treatment implications in three case reports. Int J Psychiatry Med. 2004;34(3):277-85. doi: 10.2190/VAX9-3D09-M9C7-3PA