EMA症例118:2月症例解説
2021年2月の教育班症例にご参加いただいた皆様、ありがとうございました。
ご参加いただいた皆様の属性は以下のとおりです
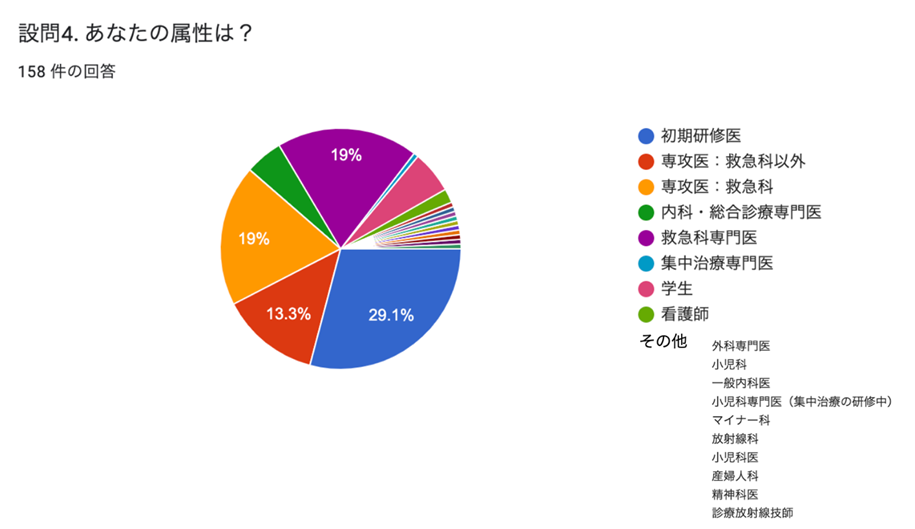
図1:回答者の属性
今回は、片頭痛の既往のある40歳女性が、3日前の雷鳴頭痛を主訴にERを受診した症例でした。真っ先にくも膜下出血を想起してくださった方が多かったのではないかと思います。
くも膜下出血は、早期に発見し脳外科医による根治治療を受けることで救命率を高めることができます。しかし画像検査が普及した現代においても、救急外来の初診時で約5%が誤診されています。動脈瘤が再破裂した場合の死亡率は60%にのぼり1)、 確実に診断することが求められます。
くも膜下出血の症状は多彩で、簡単には除外できない!Ottawa SAH Ruleの項目も参考に、CT撮影を検討しよう!
くも膜下出血が見逃される理由の第1位は頭部CTが撮影されない、つまり、くも膜下出血を疑わなかった場合です2)。sudden onsetの強い頭痛や意識障害のように典型的な病歴ばかりではなく、くも膜下出血の臨床症状はじつに多彩です。sudden onsetでなかったり、失神で来たり、頭痛が軽度だったり、自然によくなったり、NSAIDsで改善したりします。このような場合、片頭痛や筋緊張性頭痛などと誤診されてCT撮影までたどり着けないのです。その他にも嘔吐が目立って微熱を伴えば胃腸炎やウイルス性髄膜炎が疑われることがありますし、警告出血があった場合に患者さんが「先日も同じような頭痛があって自然によくなりました」と言うので「以前と同様の頭痛」としてCTが撮影されないこともあります。くも膜下出血の患者さんのCT未撮影を防ぐためはどうすれば良いでしょうか?そこでOttawa SAH Ruleを使います。
★Ottawa SAH Rule★
①40歳以上、②頚部痛または項部硬直、③目撃のある意識消失、④労作時発症、⑤雷鳴頭痛、⑥頸部屈曲制限の6項目のうち、1つも満たさなければくも膜下出血は否定できる。(感度100%、特異度12.7%)3)
Ottawa SAH Ruleは、急性の頭痛(1時間以内に痛みのピークを迎えるような頭痛)を訴える成人患者のうち、くも膜下出血の可能性がある患者を特定するためのルールです。Ottawa SAH Ruleを1項目も満たさなければ、くも膜下出血は否定的で、その精査のためにCTを撮影する必要はありません。年齢のみ該当した場合にCTを撮影するべきかは非常に悩ましいところですが、ERを受診するほどしんどい頭痛の患者さんには本当にCTが不要なのかを十分に検討する必要があります。前述のとおり、くも膜下出血の見逃しの最大の理由はくも膜下出血を鑑別に挙げずCTを撮影しなかったことですが、くも膜下出血の症状は多彩で「この頭痛はそれらしくない」とはなかなか言えないのです。感度を上げて見逃しを減らすためにはCTの閾値は下げざるをえません。CTを撮影しないとしても、患者さんにくも膜下出血であった場合のリスクを説明し、Shared decision makingに基づいてその選択をすべきでしょう。一方、病歴や所見をしっかりとチェックした上で、CTは不要という判断に至ることももちろんあります。例えば、「頭痛持ちで月に何度か救急受診する40歳の、身体所見にも引っかかる点がないいつもの頭痛」に対して、受診するたびにCTを撮影する、というのは現実的ではありませんね。Ottawa SAH Ruleについては以前に文献班でも紹介されていましたのでよろしければそちらの記事もご覧ください。https://www.emalliance.org/education/dissertation/20180104-journal
今回は、片頭痛の既往のある40歳女性が、3日前の雷鳴頭痛を主訴にERを受診した症例です。もともと片頭痛がありNSAIDsで改善しているとはいえ、40歳以上、雷鳴頭痛の2点でOttawa SAH Ruleにひっかかり頭部単純CTを撮影していますが、異常は認められませんでした。設問1では、この時点でどのような疾患を鑑別の上位にあげるかを自由記載で3つまでお答えいただきました。上位7位の結果は次のとおりです。
設問1. どのような疾患を鑑別の上位に挙げますか?(自由記載、3つまで) 208件の解答
| 1位
|
クモ膜下出血 |
93% |
|
2位 |
可逆性脳血管攣縮症候群(RCVS) |
30% |
|
3位 |
椎骨脳底動脈解離 |
28% |
|
4位 |
片頭痛 |
24% |
|
5位 |
静脈洞血栓症 |
17% |
|
6位 |
髄膜炎 |
5% |
|
7位 |
可逆性後頭葉白質脳症(PRES) 下垂体卒中 |
4% 4% |
表1:鑑別疾患の上位
頭部単純CTでくも膜下出血は認めなかったものの、やはり最も疑われたのはくも膜下出血です。そして雷鳴頭痛の原因としてコモンなRCVSが第2位に、続いて椎骨脳底動脈解離、静脈洞血栓症、PRES、下垂体卒中とコモンではありませんが雷鳴頭痛となる疾患が並んでいます。
CTの感度は6時間以内で良好、6時間以降はどんどん低下する。
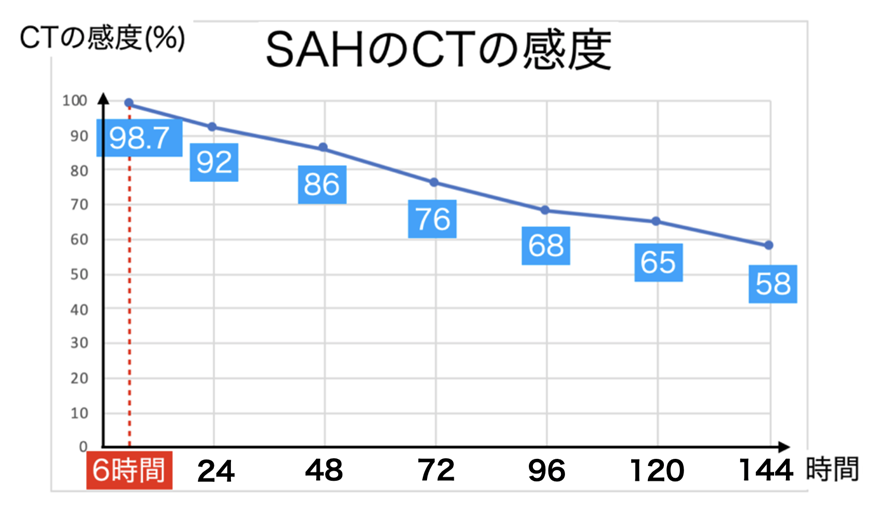
図2:くも膜下出血のCTの感度(参考文献4から作成)
国際的な前向きコホート研究において、くも膜下出血における発症6時間以内の頭部単純CTの感度は98.7%と極めて良好で、この時間帯のCTが陰性であればほぼくも膜下出血を否定できます4)。ところが、発症から時間が経つにつれて当日92%、1日後86%、2日後76%・・・5日後58% と感度が低下します。つまり6時間以降はCTの偽陰性が増えていきます。さらにこの論文では、読影者が放射線科医や経験のある脳卒中専門家であり、救急医である私達のCTの感度はこれより低いと考えます。
くも膜下出血を見逃さないためのCTのポイント:
1 シルビウス裂の左右差をみる
2 橋周囲・大脳鎌の正常の低吸収域が消失していないかをみる
3 水頭症をみる。
※③について:30%で合併する水頭症の所見がくも膜下出血のを疑う唯一のヒントになることがあります。最も早期に観察される側脳室下角の対称性拡大は人が笑っているように見えて”niko-niko sign”と言われており覚えておくとよいでしょう。
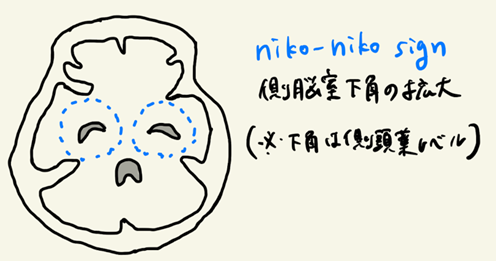
図3:niko-niko sign
今回のCTは発症3日目に撮影されたものなので、CTが陰性でもくも膜下出血は否定できません(CTの感度65-68%)。そこで、追加したい検査を設問2で選んでいただきました。その結果がこちらです。
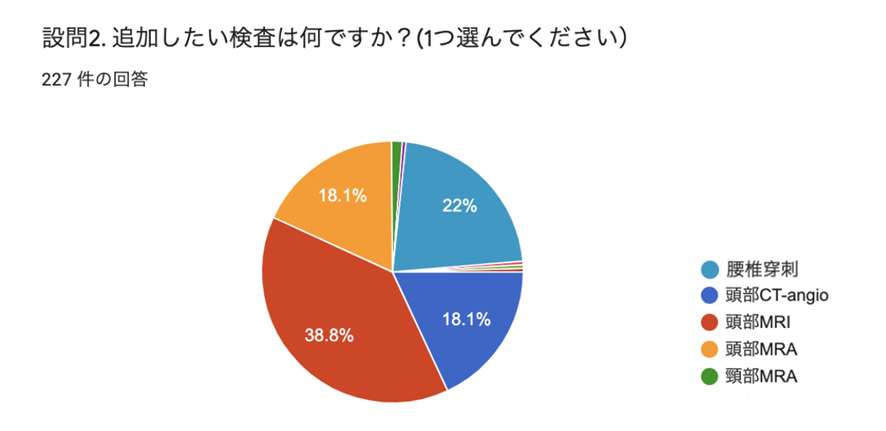
図4:追加したい検査
MRIが4割、続いて腰椎穿刺、頭部CT-angio、頭部MRAが2割程度で並んでいます。
くも膜下出血疑いでCT が陰性だったときの対応を知る
【提案(簡易版)】
発症6時間以内:CTで除外が可能
発症6時間〜24時間:腰椎穿刺 > MRI
発症24時間〜3日以内: 腰椎穿刺 and/or MRI
4日〜 MRI
くも膜下出血を疑って頭部単純CTを撮影したけれど陰性のとき、つぎの一手としてどのような検査を選択するでしょうか。アンケートの結果ではMRIを選択された方が4割と最多で、腰椎穿刺、頭部MRA、頭部CT-angioが2割前後で並びました。CTが陰性だった場合には腰椎穿刺がガイドラインで推奨されているにも関わらず、実際にはこのような解答となるのはなぜでしょうか。腰椎穿刺と最多の解答であったMRIのメリットとデメリットについて考えてみましょう。
●MRI
MRIの感度
|
|
T2* |
FLAIR |
|
発症3日以内 |
94% |
82% |
|
発症4〜14日 |
100% |
81% |
表2:MRIの感度(参考文献5から作成)
発症4日以降になるとT2*の感度が100%になるので陰性であればくも膜下出血を除外できますが、発症3日以内はMRI陰性でも6%のくも膜下出血を見逃してしまいます。またくも膜下出血のMRIを読影する機会は少なく、読影力に自信がなければ撮影しても評価は困難です。
MRIのメリット・デメリット
メリット:検査に痛みや被ばくを伴わない。日本はMRIへのアクセスが極めて良い。RCVS、椎骨脳底動脈解離、静脈洞血栓症、PRES、下垂体卒中といった鑑別の上位に上がるその他の疾患との鑑別が可能。くも膜下出血であれば動脈瘤の検索も可能。
デメリット:検査中に再破裂する危険がある。3日以内は偽陰性がある。騒音の刺激による破裂。
発症24時間以内にMRIを避けたい理由
再破裂は発症24時間以内が多く、6時間以内は特に注意が必要です。179人のくも膜下出血患者の研究では17.3%が24時間以内に再破裂を起こし、87.1%が6時間以内でした(図2参照)。6)
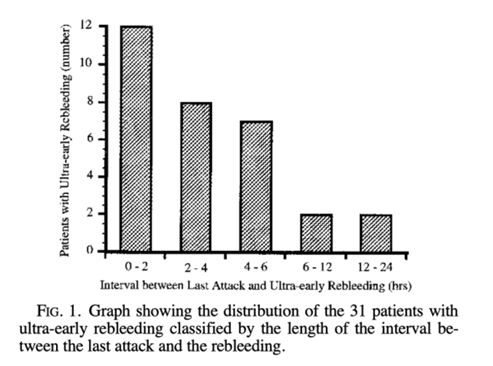
図5:発症から再破裂までの時間(参考文献6から引用)
再破裂のリスクが高い急性期は、検査時間が長く細やかな観察ができないMRIの撮影には注意が必要です。
●腰椎穿刺
腰椎穿刺のメリット・デメリット
メリット:発症2週間以内の場合頭部CT+腰椎穿刺が陰性であれば感度100%でクモ膜下出血を除外できる。患者の状態を確認しながら検査が行える。
デメリット:疼痛を伴う。25%でtraumatic tapが起こるため血性髄液かどうかの判断が困難。肉眼的キサントクロミーは分光測定法と比べて感度が低い。
<血性髄液かtraumatic tapか>
キサントクロミーがみられればくも膜下出血の診断が可能ですが、発症12時間以内は17%で偽陰性が起こります7) 。12時間以内でも血性髄液が得られればくも膜下出血と診断したいところですが、traiumatic tapは25%とかなり高頻度で起こるためくも膜下出血なのかtraumatic tapなのか判別は困難です。よく言われているスピッツ3本採取して赤血球が減少すればtraumatic tapではないと言われているのは誤りでこの方法で区別することもできません8)。一方でキサントクロミーがなく赤血球<2,000×106/Lであればtrauma tapで動脈瘤性くも膜下出血は否定できる(感度100%、特異度92.1%)と報告されており、該当症例に限っては除外可能です9)。
<肉眼的キサントクロミーの感度は低い>
キサントクロミーについても注意が必要で、分光測定法の感度は83-89%と良好ですが、肉眼的キサントクロミーでは47-67%と低下します7)。ほとんどの施設では肉眼で評価されているので知っておく必要があります。
これらのMRI、腰椎穿刺の特性から、病歴からくも膜下出血が疑われるCTは陰性だった場合の検査について以下のような考え方を提案します。
|
発症6時間以内 |
CTで除外可能 |
|
発症6時間〜24時間 |
腰椎穿刺 > MRI(再破裂リスクが高い時期) |
|
発症24時間〜3日以内 |
腰椎穿刺 and or MRI(MRI陰性で除外はできない) |
|
発症4日〜 |
MRI(MRIT2*の感度100、MRIで除外可能) |
表3:発症時間別 くも膜下出血疑いの患者への検査
検査の感度や再破裂のリスクを踏まえた案ではありますが、あくまで一つの提案です。施設によって、検査へのアクセス(時間帯によって違うかもしれません)、専門家の体制(脳外科の先生にすぐ診てもらえるか、読影できる専門家がいるか)なども違うと思いますので、自施設の関連する部門で相談し、ある程度コンセンサスを作っておくことが有用と考えます。
今回の症例は、発症3日以内で、腰椎穿刺を選択しました。そこで血性髄液を認め、くも膜下出血が強く疑われました(分光測定装置はなく肉眼的キサントクロミーは陰性でした)。24時間以内は上記理由で特にMRIより腰椎穿刺を優先していますが、3日以内であればMRIで診断してもいいし、MRI陰性で腰椎穿刺をしてもいいと思います。
設問3.で次に何をするかを自由記載でお答えいただきました。 (145件の解答)
結果は次の通りです。
|
1位 |
脳神経外科コール CT-angio |
31% 31% |
|
3位 |
MRA |
10% |
表4:次にすること
他、鎮痛・降圧、止血剤投与などのご意見をいただきました。
今回の症例では、動脈瘤の検索目的でCT-angioを撮影し、左内頚動脈後交通動脈分岐部に動脈瘤を認めました。動脈瘤性くも膜下出血と診断し、鎮痛・ 降圧を開始してオンコールの脳神経外科にコンサルトしました。
止血剤については、動脈瘤性のくも膜下出血に対してトラネキサム酸の早期投与は予後を変えない10)という結果が出ていていました。興味深いですね。
Take home message
くも膜下出血の症状は多彩で、簡単には除外できない!Ottawa SAH Ruleの項目も参考に、CT撮影を検討しよう!
・CTの感度は6時間以降はどんどん低下する。6時間以降はCT陰性でもくも膜下出血は除外できない!
・CT陰性のときは、発症からの時間による再破裂のリスクやMRIの感度を考慮し、腰椎穿刺かMRIかを選択しよう!
参考文献
1) van Donkelaar CE, Bakker NA, Veeger NJ, Uyttenboogaart M, Metzemaekers JD, Luijckx GJ, Groen RJ, van Dijk JM. Predictive Factors for Rebleeding After Aneurysmal Subarachnoid Hemorrhage: Rebleeding Aneurysmal Subarachnoid Hemorrhage Study. Stroke. 2015 Aug;46(8):2100-6. doi: 10.1161/STROKEAHA.115.010037. Epub 2015 Jun 11. PMID: 26069261.
2) Kowalski RG, Claassen J, Kreiter KT, Bates JE, Ostapkovich ND, Connolly ES, Mayer SA. Initial misdiagnosis and outcome after subarachnoid hemorrhage. JAMA. 2004 Feb 18;291(7):866-9. doi: 10.1001/jama.291.7.866. PMID: 14970066.
3) Perry JJ, Sivilotti MLA, Émond M, Hohl CM, Khan M, Lesiuk H, Abdulaziz K, Wells GA, Stiell IG. Prospective Implementation of the Ottawa Subarachnoid Hemorrhage Rule and 6-Hour Computed Tomography Rule. Stroke. 2020 Feb;51(2):424-430. doi: 10.1161/STROKEAHA.119.026969. Epub 2019 Dec 6. PMID: 31805846.
4) JKassell NF, Torner JC, Haley EC Jr, Jane JA, Adams HP, Kongable GL. The International Cooperative Study on the Timing of Aneurysm Surgery. Part 1: Overall management results. J Neurosurg. 1990 Jul;73(1):18-36. doi: 10.3171/jns.1990.73.1.0018. PMID: 2191090.
5) Mitchell P, Wilkinson ID, Hoggard N, Paley MN, Jellinek DA, Powell T, Romanowski C, Hodgson T, Griffiths PD. Detection of subarachnoid haemorrhage with magnetic resonance imaging. J Neurol Neurosurg Psychiatry. 2001 Feb;70(2):205-11. doi: 10.1136/jnnp.70.2.205. PMID: 11160469; PMCID: PMC1737199.
6) Fujii Y, Takeuchi S, Sasaki O, Minakawa T, Koike T, Tanaka R. Ultra-early rebleeding in spontaneous subarachnoid hemorrhage. J Neurosurg. 1996 Jan;84(1):35-42. doi: 10.3171/jns.1996.84.1.0035. PMID: 8613833.
7) Chu K, Hann A, Greenslade J, Williams J, Brown A. Spectrophotometry or visual inspection to most reliably detect xanthochromia in subarachnoid hemorrhage: systematic review. Ann Emerg Med. 2014 Sep;64(3):256-264.e5. doi: 10.1016/j.annemergmed.2014.01.023. Epub 2014 Mar 11. PMID: 24635988.
8) Heasley DC, Mohamed MA, Yousem DM. Clearing of red blood cells in lumbar puncture does not rule out ruptured aneurysm in patients with suspected subarachnoid hemorrhage but negative head CT findings. AJNR Am J Neuroradiol. 2005 Apr;26(4):820-4. PMID: 15814927.
9) Perry JJ, Alyahya B, Sivilotti ML, Bullard MJ, Émond M, Sutherland J, Worster A, Hohl C, Lee JS, Eisenhauer MA, Pauls M, Lesiuk H, Wells GA, Stiell IG. Differentiation between traumatic tap and aneurysmal subarachnoid hemorrhage: prospective cohort study. BMJ. 2015 Feb 18;350:h568. doi: 10.1136/bmj.h568. PMID: 25694274; PMCID: PMC4353280.
10) Post R, Germans MR, Tjerkstra MA, Vergouwen MDI, Jellema K, Koot RW, Kruyt ND, Willems PWA, Wolfs JFC, de Beer FC, Kieft H, Nanda D, van der Pol B, Roks G, de Beer F, Halkes PHA, Reichman LJA, Brouwers PJAM, van den Berg-Vos RM, Kwa VIH, van der Ree TC, Bronner I, van de Vlekkert J, Bienfait HP, Boogaarts HD, Klijn CJM, van den Berg R, Coert BA, Horn J, Majoie CBLM, Rinkel GJE, Roos YBWEM, Vandertop WP, Verbaan D; ULTRA Investigators. Ultra-early tranexamic acid after subarachnoid haemorrhage (ULTRA): a randomised controlled trial. Lancet. 2021 Jan 9;397(10269):112-118. doi: 10.1016/S0140-6736(20)32518-6. Epub 2020 Dec 23. PMID: 33357465.
最後までお読みいただきありがとうございました!
アンケートにご協力いただければ幸いです。