EMA症例150:12月解説
2023 年12 月症例にご参加いただきました皆様、誠にありがとうございます。12月21日時点で質問に回答をいただいた方は 169 名いらっしゃいました。皆様の回答の集計結果を紹介します。
質問1:鑑別診断は?(複数選択可、3つまで)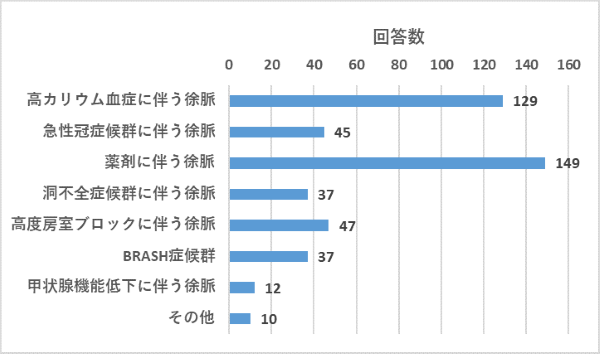
高カリウム血症および薬剤に伴う徐脈が最も疑われていました。その他の各種鑑別疾患にはほぼ均等に意見が分かれています。
質問2:優先的に確認したい追加事項はなんですか?(複数選択可、3つまで)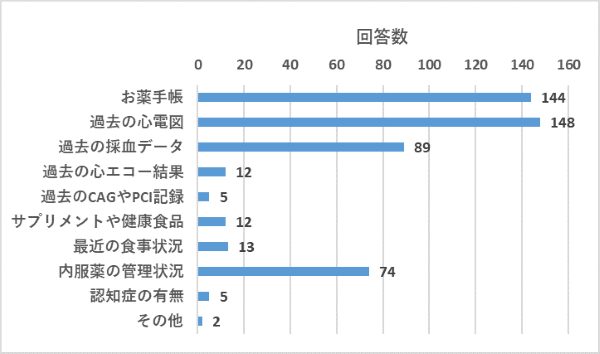
薬剤に関する情報、ならびに過去の心電図や採血データなどベースラインに関する情報を求める声が多かったです。内服薬の管理状況に関する関心が高かったのは、高齢者救急における皆様のプラクティスを反映していると思いました。
質問3:優先的に実施したい治療はなんですか?(複数選択可、3つまで)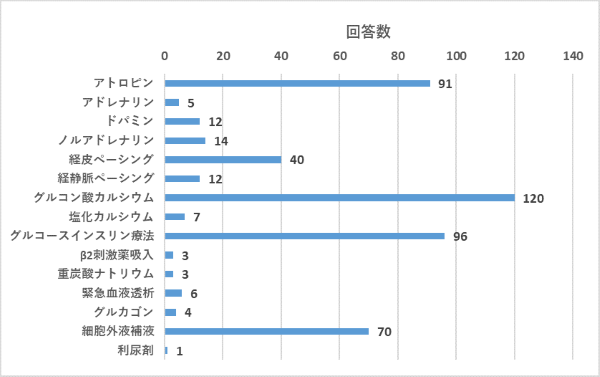
治療はアトロピン、グルコン酸カルシウム、グルコースインスリン療法、細胞外液補液の4つに意見が集約しています。またcrashしかかっている循環に対して、カテコラミンの使用よりはペーシングを使用したいという声が多かったです。
さて、本症例は皆様お気付きの通り症候性徐脈のケースです。高カリウム血症に加えて、徐脈を来す内服薬を飲んでいる、そして腎機能が悪いと、高齢者救急においてよく見かける状況かと思います。本日はこのケースを通じて、この数年で報告が増えているBRASH症候群について取り上げたいと思います。皆様はBRASH症候群をご存知でしょうか?
▼ BRASH症候群とは?
BRASH症候群とは、Bradycardia, Renal failure, AV nodal blockade, Shock, Hyperkalemia(「徐脈」「腎不全」「房室結節遮断」「ショック」「高カリウム」)の頭文字から命名された症候群です1)。BRASH症候群は上記の5つの臨床症状および病態を全て同時に兼ね備える点が特徴です。この症候群の概念は1986年にcase reportとして初めて報告されましたが2)、実際にBRASH症候群として命名されたのは2016年になります。
BRASH症候群の病態生理学的なポイントは、高カリウム血症と房室結節遮断薬が相乗して徐脈を引き起こすことにあります1)。高カリウム血症および房室結節遮断の効果を持つ薬剤は共に徐脈を引き起こしますが、これら2つの因子が同時に存在した場合には、どちらか1つの因子から予想されるよりも高度な徐脈を引き起こすと言うのです。1+1=2ではなく、3にも4にもなるということです。この現象は1990年代に動物実験で確認されていました3)。
そして、この徐脈が循環不全を招き、腎不全を悪化させ、高カリウム血症と内服薬の排泄不全を引き起こします。この結果、さらに循環不全が惹起され、腎不全が悪化し、高カリウムおよび内服薬の排泄不全という負のスパイラルが発生します。BRASH症候群は”負のスパイラル”と”相乗効果”によって臨床状況を悪化させる病態なのです。
疾患概念をイラストに示すと下記のようになります。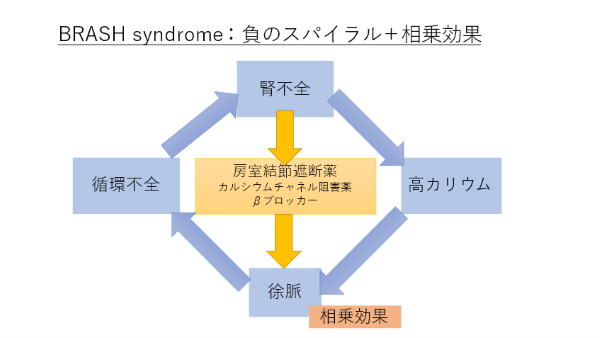
▼ なぜBRASH症候群を認識する必要があるのか?
上記の病態を聞いて、「そんなケースたまに診るし、マネジメント困ってないよ。」と思うかもしれません。徐脈を伴う高カリウム血症とマネジメントしても、多くの場合は問題ないかもしれません。しかし、先ほど述べたようにBRASH症候群は高カリウム血症のみならず、”BRASH”で示された5つ全ての要素が疾患の構成要素となっているため、それぞれが治療対象になるのです4)。単一の介入(例えば高カリウム血症としてのマネジメント)ではなく、複数の問題(高カリウムと徐脈と腎不全)に同時に対処をすることが出来れば、理論上はより早く患者さんの状態が安定することが期待されます。即ち、非侵襲的な治療を数多く行うことでペーシングや血液透析などの侵襲的な治療を回避出来る可能性があると考えられるのです。
▼ pureな高カリウム血症とBRASH症候群はどのように見分けるのか?
BRASH症候群を認識する必要性についてご説明させて頂きました。さて次は具体的にどのようにpureな高カリウム血症のケースとBRASH症候群を見分けるのか、という点ついて取り上げましょう。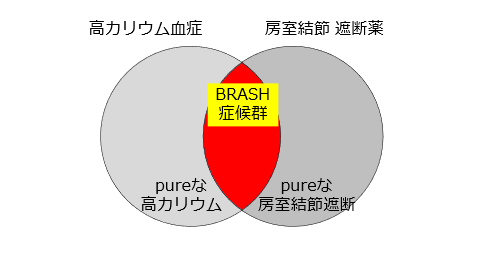
ずばり、鑑別のポイントは、”心電図変化”と”カリウムの絶対値”にあります。
まず心電図変化についてです。純粋な高カリウム血症では、テント状T波やP波の減高(消失) 、PQ時間の延長、wide QRSといった心電図変化が出現すると言われています。純粋な高カリウム血症ではこれらの所見と共に徐脈が発生することが一般的です。一方BRASH症候群の場合は、これら高カリウム血症特有の心電図所見を伴わずに房室伝導の遅れを伴う徐脈のみを呈することが多いとされます2)。この点が”相乗効果”による高度徐脈を示していると言える点で鑑別点となります。
またカリウムの絶対値も鑑別のポイントとなります。BRASH症候群ではカリウムの絶対値はmildなケースが多いと言われています。BRASH症候群の報告をまとめたレビュー文献1)によれば、カリウム値が6台の症例が最も多く、5台でも重篤な徐脈を伴ったケースもあるとされています。一方で純粋な高カリウム血症のケースでは、高カリウムの程度はsevereで一般的には7を超えると言われています。
まとめますと、徐脈を診たら心電図とカリウムをチェックすると思いますが、その際に高カリウムの心電図が揃っているか、そしてカリウムの絶対値はどれ位か、ということをきっかけにBRASH症候群を疑うことが可能となります。提示した症例の12誘導心電図においても、P波は消失せずテント状T派も認めませんでした。QRS幅の延長も伴っていません。非特異的なST変化がありましたが、高カリウム血症に特徴的な所見とは考えられませんでした。一方で、カリウムの値は6.1mEq/Lとmildな高カリウム血症でした。これらの所見を総合すると、本ケースはBRASH症候群のケースであったと考えられます。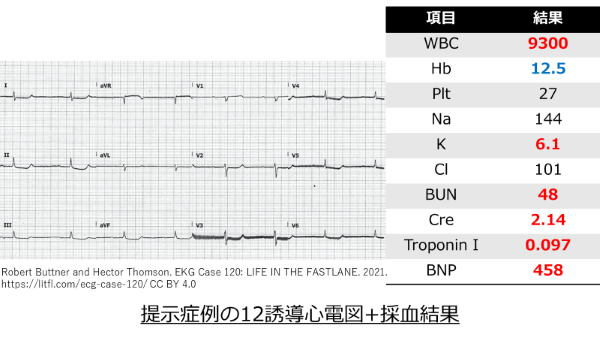
▼ BRASH症候群のトリガーは何か?
BRASH症候群は慢性心不全や高血圧症、頻脈性不整脈などを基礎疾患に持ち、各種内服薬がある患者において発生します。例えば、慢性心不全の患者ではfantastic fourと呼ばれるβ遮断薬、ARNI(アンジオテンシン受容体ネプリライシン阻害薬)、MRA(抗アルドステロン受容体拮抗薬)、SGLT2阻害薬が内服薬に入っている事が多いです。これら治療上必要なポリファーマシー状態がBRASH症候群の発生要因になるのです。
これらの多剤内服状態の患者でintake不足による脱水などが生じると、脱水をトリガーとしてBRASH症候群が生じると考えられています。脱水が急性腎不全を引き起こし、BRASH症候群の負のスパイラルが始まるのです。現在は冬季ですが、夏場には重度の徐脈患者が増えるとの報告5)があり、脱水がBRASH症候群と関連していることが示唆されています。また降圧剤の増量やスピロノラクトンなどのカリウム保持性利尿剤の増量などがトリガーになったとの報告もあります。腎不全、高カリウム、低血圧、徐脈のきっかけになりうるトリガーがなかったかどうか情報を集めることが、再発防止のために重要です。
今回のケースでは、慢性腎不全およびfantastic four薬剤含むポリファーマシー状態の背景があったところに、整形外科で開始されたNSAIDsが腎不全を引き起こし、BRASH症候群を発症したと考えられました。
▼ BRASH症候群のマネジメントは?
前半部分でも述べましたが、BRASH症候群は”負のスパイラル”が”相乗効果”により生じる疾患になります。マネジメントは単一病態への介入のみならず、総合的にマネジメントすることが良いとされています。まさにER医の腕の見せ所ですね。BRASH症候群患者を徐脈マネジメントの代表格であるACLS2020 徐脈アルゴリズム6)で対応した場合、アトロピン→効果無ければ経皮ペーシングorドパミンorアドレナリンとなりますが、これでは高カリウム血症のマネジメントを含むことが出来ません。
現時点でエビデンスレベルの高いBRASH症候群のマネジメント法は確立していませんが、下記のような治療を含むことが良手とされています。
① 高カリウム血症への対応
BRASH症候群では高カリウム血症がmildであっても、積極的に高カリウム血症の治療を行うことが勧められています7)。従ってまずは心電図変化を伴う高カリウム血症としてカルシウム製剤の投与を行います。またグルコース/インスリン療法は速やかにカリウムを細胞内にシフトさせる効果を持ち、容易に実施可能です。また頻脈作用を有するβ刺激薬の吸入もBRASH症候群では理にかなった選択肢となります。カリウムを体外に排泄する利尿剤の使用も検討されますが、後述する体液量の評価を合わせて行うことが大切です。
② 徐脈への対応
高カリウム血症を伴う徐脈に対してはカルシウム製剤の投与が1st choiceですが、残念ながら反応が得られなかった場合には、アドレナリンの使用を積極的に検討するのが良いとされています。理由は2つあります。1つはアドレナリンが心拍数と心拍出量を共に増加させる作用を有していること、もう1つはカリウムを細胞内にシフトさせる効果を有していることです。アドレナリン以外の候補としてイソプロテレノール(プロタノール)も良いですね。イソプロテレノールは純粋なβ作用のみを有し、血圧上昇作用は有さず心拍数のみを上げる薬剤と認識されています。
ACLS2020における徐脈アルゴリズムの1st choiceであるアトロピンは、BRASH症候群には効果が乏しいものと予想されます。前述した通りBRASH症候群の病態は房室伝導の低下にありますので、洞結節の興奮頻度を増加させるアトロピンではこの問題を解決出来ないと考えられるからです。しかしこれはアトロピン投与の回避を推奨しているわけではありません。投薬禁忌には該当しませんので、他の不整脈のとの鑑別を進める上でもまずアトロピン投与を実施しても良いと思われます。
③ 輸液による蘇生
BRASH症候群では脱水がトリガーになることが多く、Fluid resuscitationが必要となることが多いとされます。しかし一方で腎不全のために乏尿となり、溢水に至っているケースも考えられます。患者の体液量および血管内Volumeを評価し、患者に応じた輸液戦略が必要となります。
基本的には重炭酸リンゲル液や酢酸リンゲル液などのbalanced crystalloidを使用することになりますが、腎不全によるアシドーシスおよび高カリウム血症がある状況であれば蘇生輸液に炭酸水素ナトリウム(メイロン)を混合して輸液を行うことも理にかなっていると思われます8)。アシドーシスの改善によりカリウムが細胞内シフトすることが期待されます。
④ 房室結節遮断薬中毒への対応
最後に房室結節遮断薬の血中濃度上昇に対するマネジメントはどのようにしたらよいのでしょうか?一般的には、これらの現象を引き起こす薬剤として、カルシウムチャネル阻害剤(CCB)およびβブロッカー(BB)が有名です。CCBおよびBB中毒に対しては、グルカゴンや高容量インスリン/グルコース療法(高カリウム時のGI療法と投与量が異なるので注意)、脂肪乳剤などが治療選択肢として挙げられています9)。CCB中毒では高カリウムのマネジメントでも登場したカルシウム製剤投与も効果的とされています(ただし、カルシウム製剤も高カリウム時とCCB中毒時には推奨投与量が異なるので注意)。BRASH症候群の患者は単一の薬剤ではなく、複数の薬剤の副作用が出現しやすいことが特徴的であり、単一の薬剤をターゲットとせず複数の薬剤に対するマネジメントを要する可能性が高いです。
ただし、現在のBRASH症候群をまとめた文献によれば、基本的にはBRASH症候群では意図的な過量服薬のケースではないので、中毒マネジメントが果たす役割は大きなものではないのではないかとされています1)。上記の①~③の対応を取ってもなお、反応しない重症例において治療オプションとして持ち合わせるのが良いと現時点では考えられます。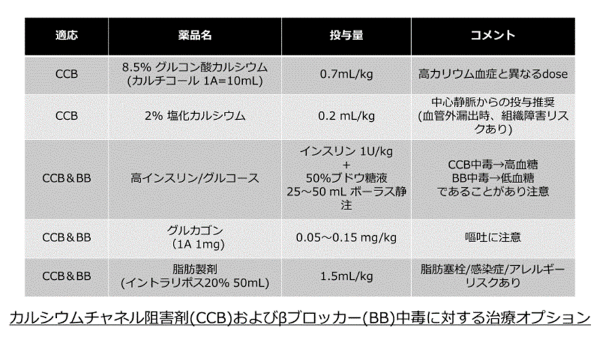
以上、簡単ではありますがBRASH症候群のマネジメントに関するOverviewになります。当然、患者の状態がCrashしている場合にはペーシングや時によってはECMO含む体外循環も検討されるでしょう。しかしながら、ALCS徐脈アルゴリズムを超えて、患者の病態を理解した上で複合的な治療を行うことでBRASH症候群患者の状態を少しでも早く改善させることが期待されます。現時点ではBRASH症候群のbest practiceはまだ不明な点も多く、これからの症例集積により知見が明らかにされることが期待されます。
最後に今回の学習ポイントのまとめです。
① BRASH症候群を理解する
② BRASH症候群のトリガーについて理解する
③ BRASH症候群のマネジメントについて理解する
いかがだったでしょうか?今回はBRASH症候群という、経験したことがあるけど、なんとなく見逃していたかもしれないポリファーマシーに関連するケースを取り上げました。今回のケースをきっかけにBRASH症候群がより理解され、皆様の日々の診療に役立つことを期待しております。
〈EM Crit〉 https://emcrit.org/pulmcrit/brash-syndrome-bradycardia-renal-failure-av-blocker-shock-hyperkalemia/
〈LITFL〉https://litfl.com/brash-syndrome/
参考文献
1) Farkas JD, Long B, Koyfman A, Menson K. BRASH Syndrome: Bradycardia, Renal Failure, AV Blockade, Shock, and Hyperkalemia. J Emerg Med. 2020;59(2):216-223. doi:10.1016/j.jemermed.2020.05.001
2) Lee TH, Salomon DR, Rayment CM, Antman EM. Hypotension and sinus arrest with exercise-induced hyperkalemia and combined verapamil/propranolol therapy. Am J Med. 1986;80(6):1203-1204. doi:10.1016/0002-9343(86)90688-1
3) Jolly SR, Keaton N, Movahed A, Rose GC, Reeves WC. Effect of hyperkalemia on experimental myocardial depression by verapamil. Am Heart J. 1991;121(2 Pt 1):517-523. doi:10.1016/0002-8703(91)90720-3
4) Farkas J. BRASH syndrome: Bradycardia, Renal failure, Av blocker, Shock, and Hyperkalemia. Pulmcrit (EMCrit). 2016.
Available at: https://emcrit.org/pulmcrit/brash-syndrome-bradycardia-renal-failure-av-blocker-shock-hyperkalemia/.
5) Palmisano P, Accogli M, Zaccaria M, et al. Relationship between seasonal weather changes, risk of dehydration, and incidence of severe bradyarrhythmias requiring urgent temporary transvenous cardiac pacing in an elderly population. Int J Biometeorol. 2014;58(7):1513-1520. doi:10.1007/s00484-013-0755-7
6) Panchal AR, Bartos JA, Cabañas JG, et al. Part 3: Adult Basic and Advanced Life Support: 2020 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation. 2020;142(16_suppl_2):S366-S468. doi:10.1161/CIR.0000000000000916
7) Wooten JM, Kupferman FE, Kupferman JC. A Brief Review of the Pharmacology of Hyperkalemia: Causes and Treatment. South Med J. 2019;112(4):228-233. doi:10.14423/SMJ.0000000000000957
8) Blumberg A, Weidmann P, Ferrari P. Effect of prolonged bicarbonate administration on plasma potassium in terminal renal failure. Kidney Int. 1992;41(2):369-374. doi:10.1038/ki.1992.51
9) 早川 桂. 循環作動薬中毒. INTENSIVIST. 2017;9(3):657-667