EMA症例145:7月解説
2023年7月症例の解説です。今月の症例は、いかがだったでしょうか。
たくさんのご回答をいただき、ありがとうございました。
今回のポイントはズバリ『血液凝固線溶系検査のミ・カ・タ』です!
ERで出血関連のプロブレムがあると提出される【血液凝固線溶系検査】ですが、、、意外と誰かに教えてもらったり、自分自身で勉強したりする機会は少ないのではないかと思います。せっかくの機会なので、ERでの血液凝固線溶系検査について勉強していきましょう。
症例は・・・
半年前から身に覚えのない皮下出血を自覚するようになった高齢女性です。腹痛を主訴に来院しましたが、四肢の紫斑や左側腹部膨隆などがみられ、血液検査では血液凝固異常があるという症例でした。
皆さんの症例へのアプローチを見ながら、解説していきましょう!
質問1: 追加したい検査はありますか?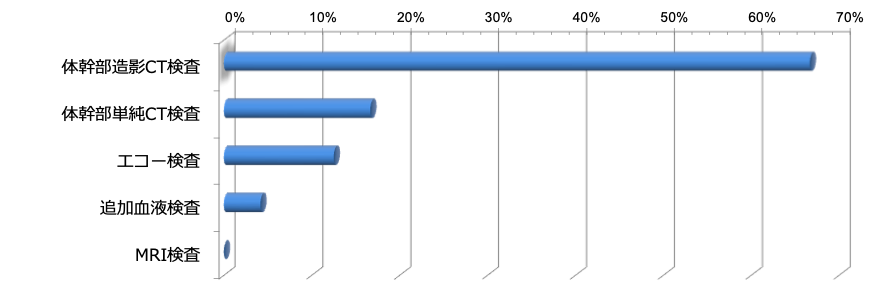
追加したい検査として、多くの方が体幹部造影CT検査を挙げていました。では、どこでそのような判断をした方が多かったのでしょうか?腹痛で来院した高齢女性に四肢の紫斑と左側腹部膨隆があるだけでなく、血液凝固異常としてPlt 6.6 万/μLと血小板低下、D-dimer 41.3 µg/mLと線溶亢進がみられ、Hb 8.7 g/dLと軽度貧血を認めることから出血が浮かんだ方が多かったのではないでしょうか?なぜ、これで出血を想起するのか理屈を含めて少しだけ深掘りしていこうと思います。長くなりますが、『血液凝固線溶系検査のミ・カ・タ』のポイントとなりますのでご参考にしてください。
【血液凝固線溶系検査とは】
止血凝固能(=出血しやすいか、血が止まりにくいか)を評価する検査には、大きく分けて血小板系と凝固線溶系の2つがあります。前者は血小板数をチェックし、後者の凝固線溶系検査はプロトロンビン時間(PT)や活性化部分トロンボプラスチン時間(APTT)、フィブリノゲン、フィブリン・フィブリノゲン分解産物(FDP)、D-ダイマーなどでチェックします。
<血小板系検査>
一般的には血小板数が5万/μL以上あれば、出血傾向は現れないとされています。また、血小板「数低下」でなく血小板「機能低下」で出血傾向を来たすものがあり、代表的な疾患が血小板機能異常症です。
では、血小板「数低下」が出血傾向につながるのはどういう病態でしょうか?ズバリ、数そのものではなく、血小板数が減っている原因が重要です。例えば、血液疾患(再生不良性貧血や骨髄異形成症候群など)での血小板の「産生不良」では、血小板数が1〜2万/μLと低下してもそれだけで出血することは少ないです。反対にDIC(線溶亢進型)や大量出血などで消費性に血小板減少を来している病態では、血小板数が3〜5万/μL 程度でも出血傾向が現れます。このような時は血小板だけでなく、凝固線溶系異常もきたしていることが多いので合わせてチェックしましょう。本症例でも、血小板6.6万/μLと軽度の低下にも関わらず出血傾向を呈していることから、凝固線溶系検査のチェックが重要になります。
★Point 血小板減少で出血傾向を来たすかは原因による
<凝固線溶系検査>
今回は凝固線溶系検査の中でもERで一般的に検査されることが多いPT、APTT 検査ではなく(本症例でもPTとAPTTは正常範囲内)、FDP、D-ダイマーに着目したいと思います。
血管が損傷して出血すると血小板や凝固因子が関与し、損傷部分に安定化フィブリン(血栓)が形成され止血されます。そして、血管が修復され止血していた血栓が不要になると、血液の循環を維持するため線溶反応が生じ、血栓はプラスミンという酵素により分解(線溶)されます。その安定化フィブリン(血栓)が分解(二次線溶)された「フィブリン分解産物」と、止血の最終過程で重要なフィブリノゲンが分解(一次線溶)された「フィブリノゲン分解産物」との総称をフィブリノゲン/フィブリン分解産物(fibrinogen/fibrin degradation products:FDP)、二次線溶の終末分解産物をDダイマーと称します。多くの方が認識されているように、これらFDP・Dダイマーが上昇している場合、「播種性血管内凝固症 ( disseminated intravascular coagulation:DIC)」と「深部静脈血栓症(DVT)」の2つの重要な病態を想起する必要があります。
では、FDPとDダイマーは何を示しているのでしょうか?フィブリン分解産物、フィブリノゲン分解産物と紛らわしいですが、FDPは一次+二次線溶、Dダイマーは二次線溶(血栓の溶解)のマーカーとして測定されます。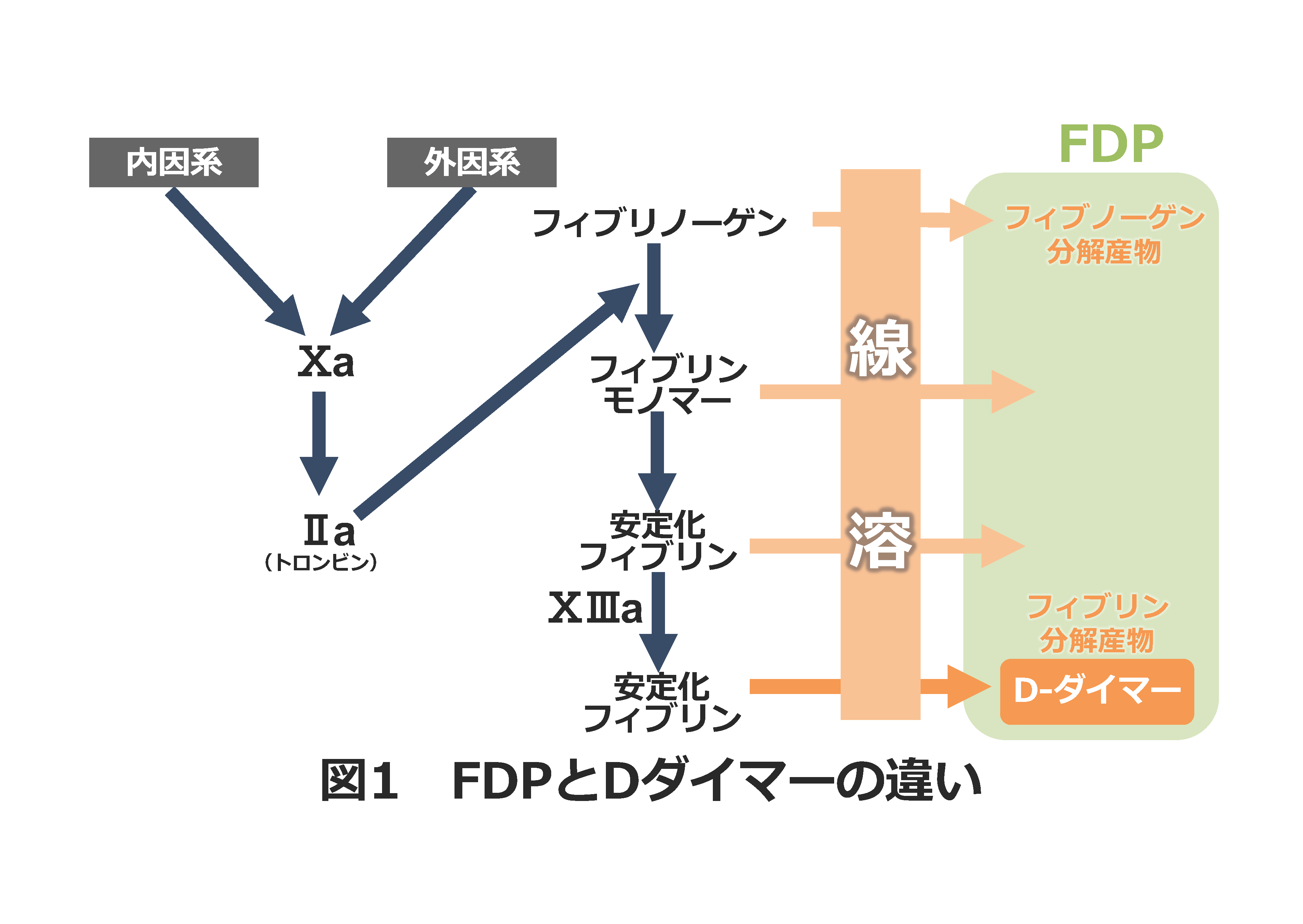
ただ、臨床的には一次線溶が亢進する場合、二次線溶亢進も混在する場合が多いです。そのため、二次線溶亢進を示すDダイマー上昇では、血栓溶解を生じる血栓症の存在を想起だけなく、一次線溶亢進も合併していないかをチェックすることは非常に重要です。特に、その場合Dダイマーが(FDPも)著明に高値になることが多いです。本症例でもD-dimer 41.3 µg/mLと著明に高値であり、一次線溶亢進の合併も疑われます。また、それは線溶亢進型DICという出血症状が前面に出るDICを疑います。本症例では、それに付け加えて四肢に紫斑が散在する点や血小板が低値であることも線溶亢進型DICを疑うポイントとなります。
★Point FDPやDダイマーの異常高値では線溶亢進型DICを考慮する
長くなりましたが、以上から出血を想起することになります。そのため、造影CT検査で出血源の検索を行うと選択された方が多かったと思われます。ただ、低侵襲なエコー検査や慢性腎臓病を考慮したと思われる単純CT検査を選択された方もいらっしゃいました。ここは、施設での方針によるところもあるかと思われます。また、追加血液検査ではFDPやフィブリノゲンの追加を考慮します(保険査定に引っかかることがあります)。
では、続いて質問2の皆さんの回答からみていきたいと思います。
質問2:上記の症例で血小板減少と筋肉内血腫を引き起こすと考えられる病態を記述してください。
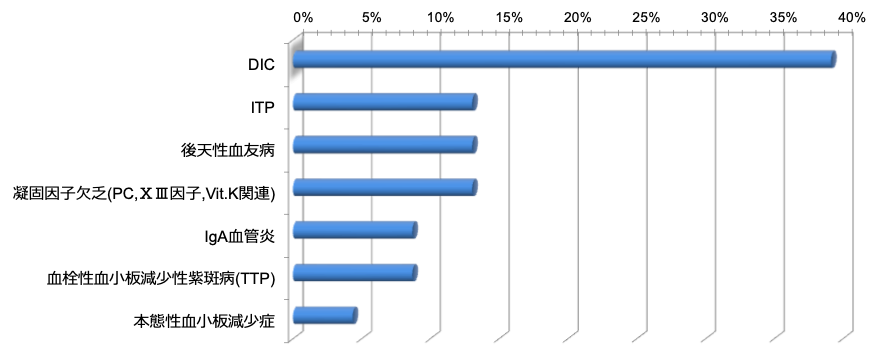
問題の続きでは、造影CT検査で左腹壁から血管外漏出像と偽腔開存型大動脈解離を認め、追加の血液検査では Fib 64 mg/dLとフィブリノゲンの著明な低下と、FDP118 µg/mLと著明な上昇がみられました。それらを踏まえて多くの方がDICと答えていました。
【線溶亢進型DIC】
DICは基礎疾患の存在下に全身性持続性の著しい凝固活性化をきたし、細小血管内に微小血栓が多発する重篤な病態です。凝固活性化と共に線溶反応もみられますが、その線溶の程度は基礎疾患によって異なり、病型は線溶抑制型と線溶均衡型、線溶亢進型に分けられます。また、臨床症状も臓器障害がメインか、出血症状がメインか、病型により大きく異なります。そして、病型はフィブリノゲン値やFDP・Dダイマーの上昇程度、Dダイマーに対するFDPの割合(FDP/Dダイマー比)である程度推測できます。DICの病型を判断することで、DICに対する抗凝固療法の選択がしやすくなります。ただ、DIC 治療において病型に関係なく、最も重要なのが基礎疾患に対する治療です。産科 DIC で原因の除去後に速やかに DIC が改善したり、急性白血病において化学療法と輸血治療のみでDICが改善する例もあります。
線溶亢進型DICでは、出血症状(紫斑、消化管出血、血尿など)がみられ、臓器症状はほとんどみられません。一次線溶も亢進するためフィブリン分解のみならずフィブリノゲン分解も進行し、フィブリノゲン値は低下するとともにDダイマー以上に FDP が著増しFDP/Dダイマー比は上昇します。本症例でもフィブリノゲンの著明な低下と、FDP/Dダイマー比の3倍近い上昇がみられ線溶亢進型DICと診断でき、今回の線溶亢進DICの原因は偽腔開存型大動脈解離によると考えられます。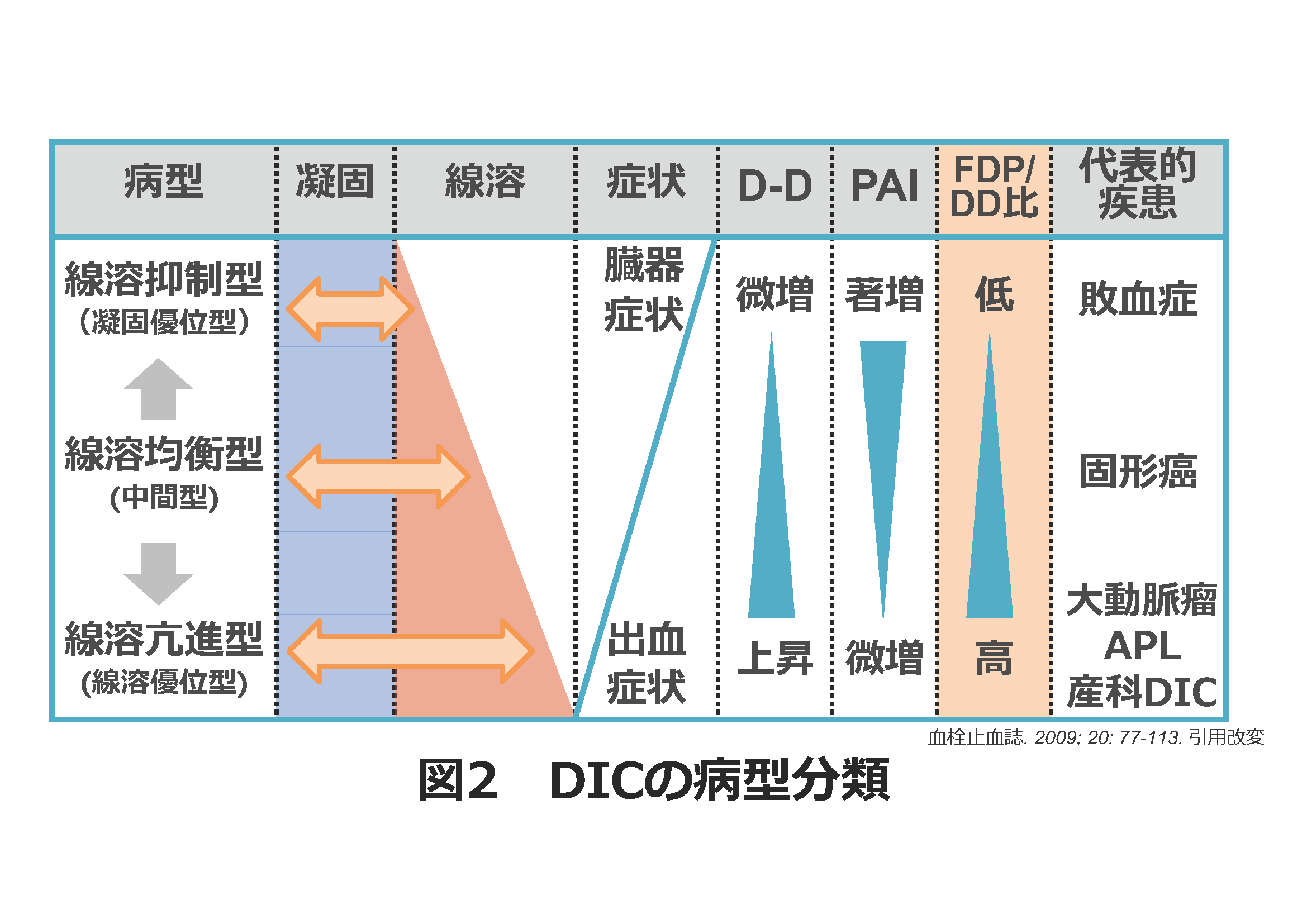
以下の疾患もDICの重要な鑑別となります。
特発性血小板減少性紫斑病(ITP)は原発性に加えてHelicobacter pylori関連やウイルス感染などの原因により、抗血小板抗体による末梢での血小板破壊亢進と骨髄での血小板産生障害をきたす疾患で、凝固異常を来たすことは少ないです。
後天性血友病は、高齢者および分娩時に多く、何らかの自己免疫学的機序により後天的に血液凝固因子に対する自己抗体が産生され、その抗体により止血が困難になる疾患です。血液検査では血小板数やPTが正常でAPTTのみが延長し、第Ⅷ因子活性や第Ⅷ因子インヒビターを測定することで診断します。高齢者での出血では念頭に置いておきます。
IgA血管炎は主に小型血管を侵す血管炎で小児に最も多く生じます。一般的な症状としては、触知可能な紫斑や関節痛、糸球体腎炎などがあります。
血栓性微小血管障害症(thrombotic microangiopathy:TMA)は、微小血管血栓により溶血性貧血と血小板減少に伴う腎臓や脳神経を中心とした臓器症状を認める疾患群です。その中にADAMTS13活性10%未満で診断される血栓性血小板減少性紫斑病(thrombotic thrombocytopenic purpura: TTP)や、志賀毒素産生性大腸菌による溶血性尿毒症症候群(hemolytic uremic syndrome: HUS)、補体系異常である非典型(atypical)HUS(aHUS)があります。
続いて、質問3も皆さんの回答からみていきたいと思います。
質問3:上記病態を踏まえて止血術以外の薬剤による治療方針を記載してください。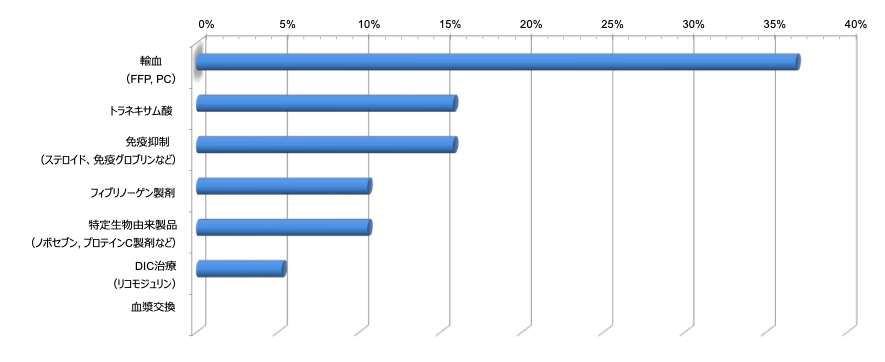
偽腔開存型大動脈解離による線溶亢進型DICと診断した後は治療方針です。多くの方が輸血を選択され、トラネキサム酸投与やフィブリノゲン製剤・特定生物由来製品投与が続きました。
線溶亢進型 DIC に対する治療として輸血やフィブリノゲン製剤投与以外に、抗線溶療法として代表的な抗プラスミン薬であるトラネキサム酸があります。トラネキサム酸はプラスミノゲンのリジン結合部位と結合してフィブリンへの結合を阻害することで抗プラスミン作用(抗線溶作用)を発揮する薬です。トラネキサム酸の最も効果を発揮する病態は「線溶亢進に伴う出血傾向」で、線溶亢進型DICが最も適していると言えます。ただ、致命的な血栓症の合併や痙攣、臓器障害の報告があり、専門家の助言のもとに行うよう推奨されています。
【本症例の経過・・・】
来院後、輸血療法(新鮮凍結血漿:FFP)やトラネキサム酸投与を行いながらIVRでの止血術を行いました。その後、血小板は上昇しFDP・Dダイマーも低下しましたが、来院4日目より再度フィブリノゲン値が低下傾向となり、FDP・Dダイマーが上昇傾向となったため、トラネキサム酸内服投与を開始しました。さらにその後は出血イベントもなく、血液検査も改善し自宅退院となりました。
【大動脈解離や大動脈瘤に伴う慢性DIC】
<概要>
大動脈瘤にDICを合併することは古くから報告されており、同様に大動脈解離に伴う慢性DICも慢性期に起こる重篤な合併症です。これらの慢性DICは、病型としては線溶亢進型DICとなり出血症状を引き起こします。抜歯や外傷などを契機に出血制御が困難となるものの、現状では明確な診断・治療指針がなく、対応に苦慮することが多いとされます。
<病態・症状>
大動脈瘤や慢性大動脈解離では瘤内部や偽腔内における壁在血栓の形成とその溶解や血液の乱流が線溶系亢進をきたすと考えられていますが、詳細は解明されていません。
症状としては出血症状がメインとしてみられることがあります。ただ、症状がはっきりせず血液検査異常のみで発見されることもあります。
<診断>
線溶亢進型DICの診断は血液検査によって確定されます。DICの検査項目には、血小板数やPT、APTT、FDP、Dダイマーなどがあります。特にPTやAPTTが正常であり、見逃されることもあります。ただ、FDPやDダイマーは著明に上昇しており、FDP/Dダイマー比が上昇し一次線溶亢進の所見がみられます。また、プラスミン–α2プラスミンインヒビター複合体(PIC)の著明な上昇やα2PI、プラスミノゲンの低下もみられます。
<治療>
線溶亢進型DICの治療は非常に難しく、まず原因となる大動脈解離そのものの治療が必要です。解離の部位や範囲、患者の全体的な状態などによって、外科手術や内科的治療が選択されます。その上で、DICの治療として出血傾向を呈しフィブリノゲンが低下している場合はFFPの補充療法や抗線溶療法などが考慮されます。ただ、これらは患者によって個別で判断されます。
抗凝固療法として未分化ヘパリンやヘパリン類(低分子ヘパリン、フォンダパリヌクス、ダナパロイド)、さらにナファモスタット,遺伝子組換えトロンボモジュリンといった薬物が用いられますが、大動脈瘤による慢性 DICに対する投与量など確立されたものはありません。一方、線溶亢進がきわめて強い場合には抗凝固療法が出血を助長するという懸念もあります。また、線溶亢進型DICではトラネキサム酸などの抗線溶療法が用いられることがあります。
最近では抗凝固療法として直接経口抗凝固薬(direct oral anticoagulant:DOAC)を用いた報告もあり、今後の知見の集積が期待されます。
以上のように、大動脈解離に伴う慢性DIC、線溶亢進型DICは複雑な病態を呈し、適切な診断と治療が重要です。患者の状態を詳細に評価し、必要な治療を迅速かつ適切に施すことで、生命を脅かす状況を改善し患者の予後を改善する可能性があります。
<まとめ>
- Dダイマー異常高値では一次線溶亢進合併(線溶亢進型DIC)を考慮する。
- DICが疑われる際には、フィブリノゲン値やFDP・Dダイマーの上昇程度、DダイマーにおけるFDPの割合(FDP/Dダイマー比)から病型分類も行う。
- 偽腔開存型大動脈解離は慢性期にDICを合併することを意識しておく。
【参考文献】
1) 日本循環器学会,日本心臓血管外科学会,日本胸部外科学会,日本血管外科学会.2020 年改訂版大動脈瘤・大動脈 解 離 診 療 ガイドライン. https://www.j-circ.or.jp/cms/wp-content/uploads/2020/07/JCS2020_Ogino.pdf (参照:2023 年7月31日)
2) Asakura H. Classifying types of disseminated intravascular coagulation: clinical and animal models. J Intensive Care. 2014;2(1):20
3) Yamada S, Asakura H. Therapeutic Strategies for Disseminated Intravascular Coagulation Associated with Aortic Aneurysm. Int J Mol Sci. 2022;23:1296.
4) Yamada S, Asakura H. Management of disseminated intravascular coagulation associated with aortic aneurysm and vascular malformations. Int J Hematol. 2021;113:15-23.
5) Fisher DF Jr, Yawn DH, Crawford ES. Preoperative disseminated intravascular coagulation associated with aortic aneurysms. A prospective study of 76 cases. Arch Surg. 1983;118:1252-1255.
6) Mendes BC, Oderich GS, Erben Y, Reed NR, Pruthi RK. False Lumen Embolization to Treat Disseminated Intravascular Coagulation After Thoracic Endovascular Aortic Repair of Type B Aortic Dissection. J Endovasc Ther. 2015;22:938-941.
7) Liu H, Liu Y, Lai J. Management of disseminated intravascular coagulation after thoracic endovascular aortic repair of type B aortic dissection: a case report. BMC Cardiovasc Disord. 2022;22:323.
8) Iida Y, Asano R, Hachiya T. Successful treatment of chronic type B aortic dissection complicated by disseminated intravascular coagulopathy with recombinant human soluble thrombomodulin after thoracic endovascular aortic repair. Vascular. 2022;30(1):38-41.
9) Kadohira Y, Yamada S, Matsuura E, et al. Aortic Aneurysm-associated Disseminated Intravascular Coagulation that Responded Well to a Switch from Warfarin to Rivaroxaban. Intern Med. 2017;56(21):2913-2917.