EMA症例134:6月症例 解説
2022年6月症例にご参加いただきました皆さま,ありがとうございました.今回のテーマは「血小板減少の鑑別と治療」です.
今回の症例では,救急外来を下痢,倦怠感のために受診した患者さんに採血検査をおこなったところ,著明な血小板減少がありました.
最初に本症例のTake home messageをお示しします.本稿を通じて,これらの3点を一緒に身につけていきましょう!
1.血小板減少+凝固障害なし+溶血性貧血あり→微小血管障害症 (TMA)を考えよう
2.感染症に合併する血小板減少は播種性血管内凝固症候群 (DIC)だけではない
3.感染治療をしてもよくならないDICでは,TMAの可能性を思い出そう
アンケート結果
まず,提示した症例から考えられる診断名をみなさんに伺ったところ,以下のような結果でした.
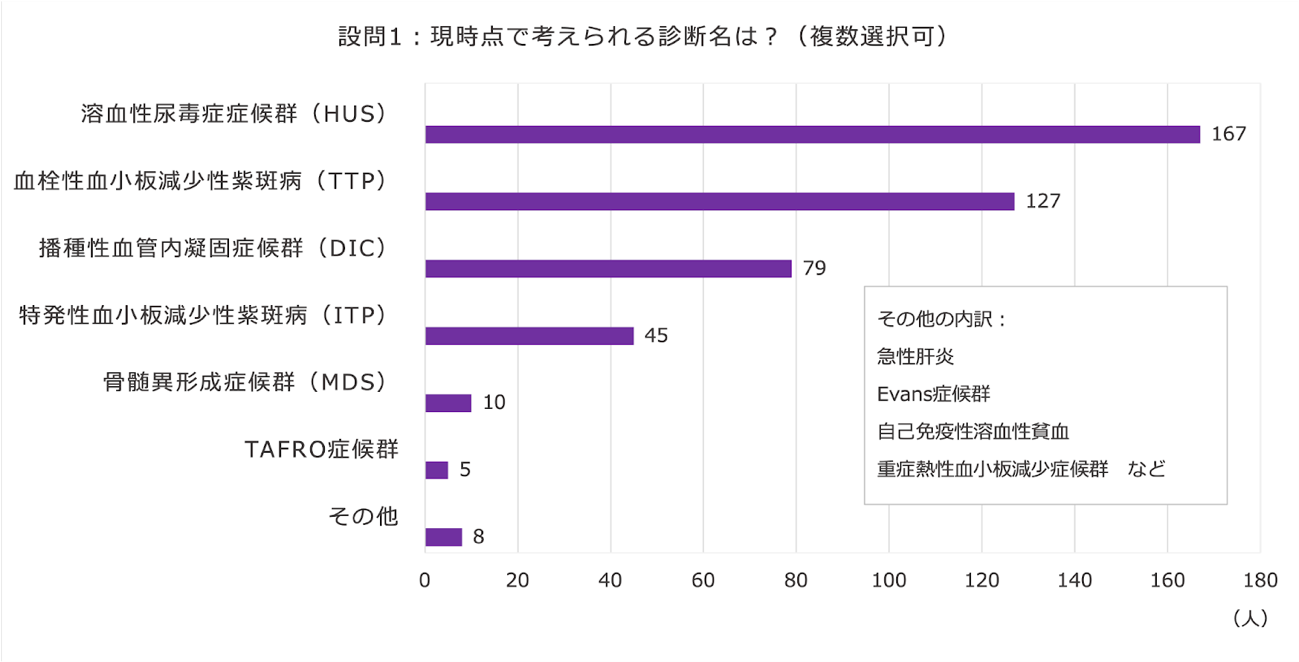
血小板減少といって思いつくのは,播種性血管内凝固症候群(DIC)ではないでしょうか.血液疾患でなければ,救急外来では肝硬変や化学療法によるものもよく診るでしょう.
DICの全人口における発症率は10万人あたり18人です(日本はDIC診断に熱心な国であり,さらに高頻度かもしれません).以下のような鑑別疾患の頻度と比べると,一般的な病態です[1].
・ 播種性血管内凝固症候群(DIC):18例/10万人
・ 血栓性血小板減少性紫斑病(TTP):6例/100万人
・ 志賀毒素産生大腸菌による溶血性尿毒症症候群(STEC-HUS):29例/100万人
・ 非典型HUS(aHUS):0.2~0.4例/100万人
しかしTTPやaHUSはDICに比べると稀ではありながらも,特異的な治療があるため,きちんと拾い上げていくことが重要です.
さて,血栓性微小血管障害症(TMA)をご存知でしょうか.細血管障害性溶血性貧血,血小板減少,細血管内血小板血栓による臓器障害を特徴とする疾患群で,TTP,STEC-HUS,aHUS,その他の二次性TMAを含んでいます(図1).
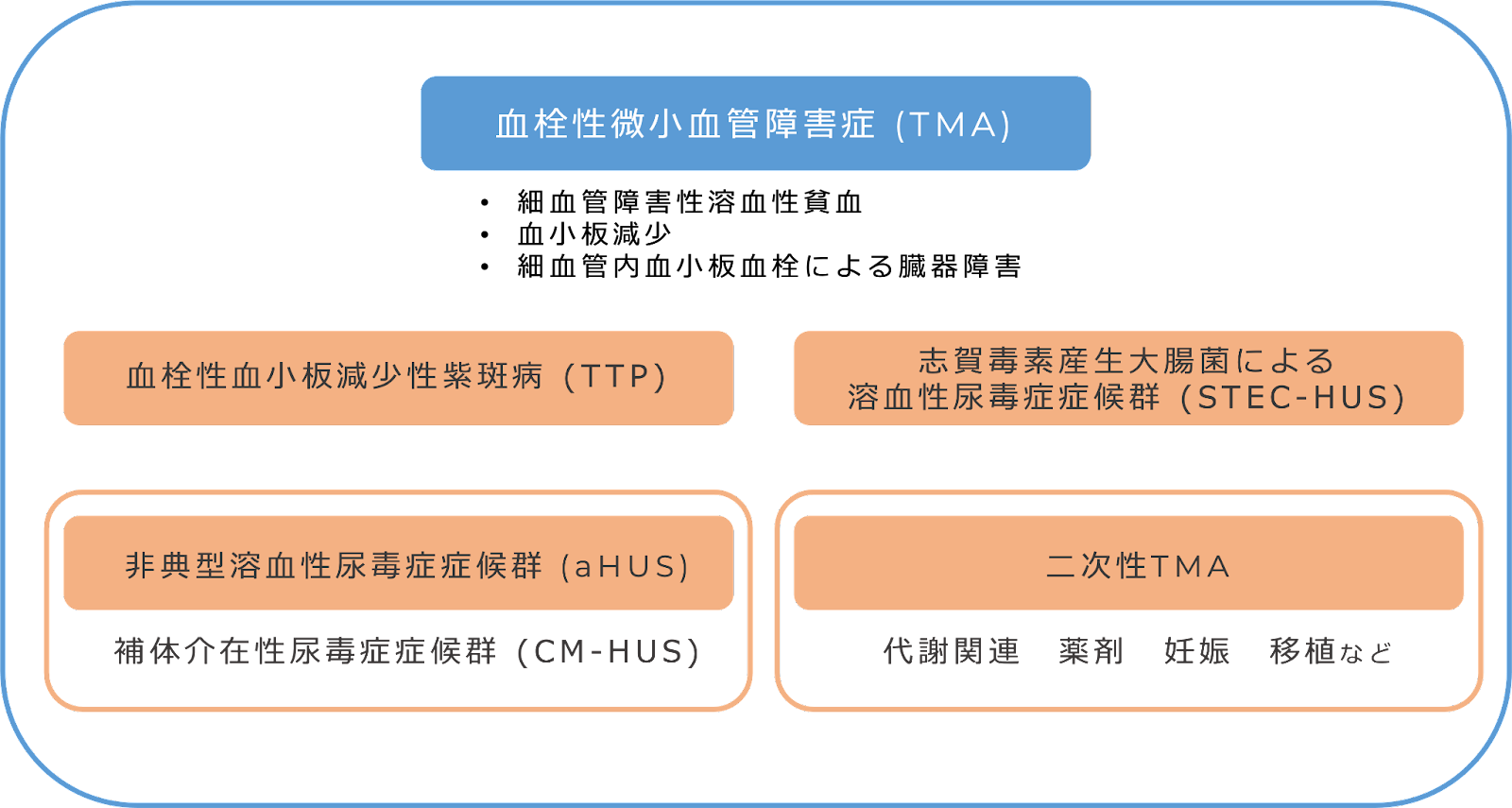
図1. TMAの概略図(文献[2]より引用改変)
代表的なDICとTMAの特徴を比較すると以下の表の通りです.
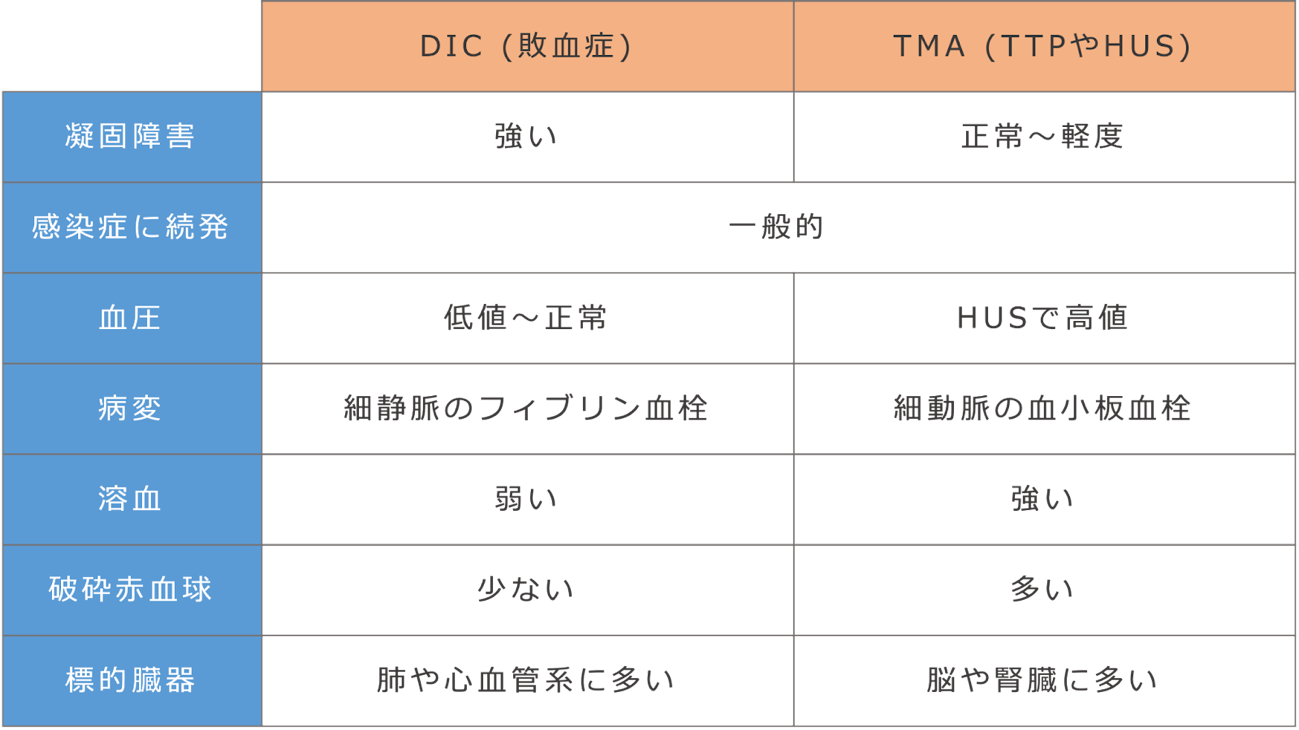
表1. 代表的なDICとTMAの比較 [1-3]
いずれも敗血症に続発しうるというところが注意点で,敗血症性DICと思いきやTTPやHUSであったということが起こりうるわけで,鑑別は容易ではありません[3].
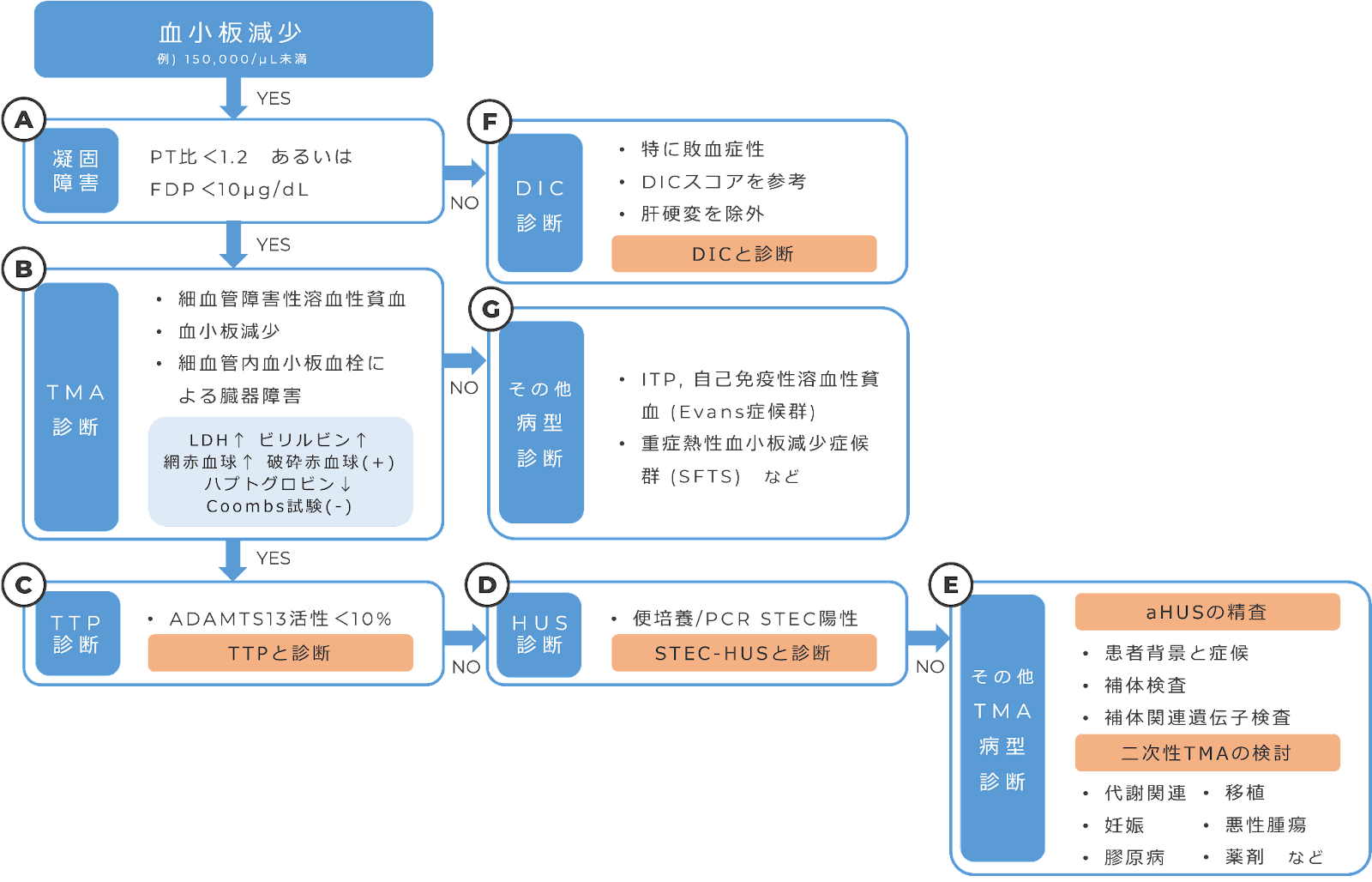 図2. 血小板減少の診療フロー(文献[1、3]より引用改変、 参考[2])
図2. 血小板減少の診療フロー(文献[1、3]より引用改変、 参考[2])
鑑別のために,図2のようなフローで血小板減少を診療することを提案します.
図2のようにクリアカットに分類できないことも多いものの,凝固異常の程度から鑑別診断をおこなうと理解しやすいです.
本症例では,PT-INR 0.98, PT% 103.2%, FDP 11.10 μg/dLと凝固異常は目立たず,図2(A)は”YES”に該当し,TMA診断に進みます.
次に症例提示の際に,みなさんには優先的におこないたい採血検査を自由記載でお答えいただきました.3件以上の回答があったものを集計しています.
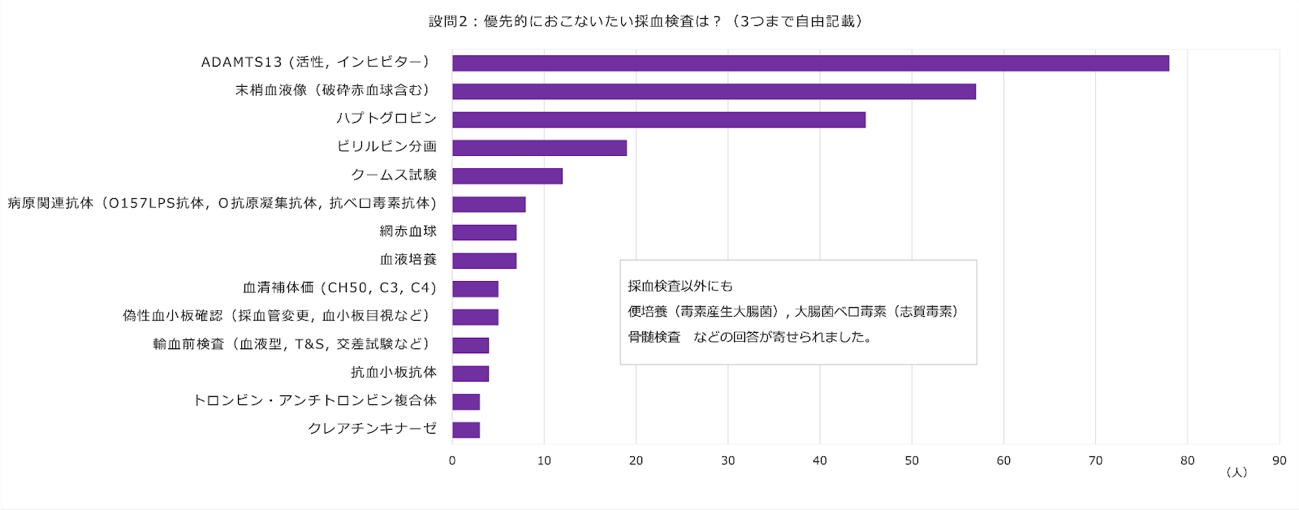
では本症例では,実際どのような追加検査をおこなったのでしょうか.追加検査の結果は表2の通りです.

表2. 今回の症例の追加検査結果
表2の結果をふまえると,図2(B)は”YES”に該当し,TMAであることがわかりました.
次はTMAの病型を鑑別していくことになります.最も注目するのは,ADAMTS13活性が正常であることで,TTPが否定的であることです.ただしADAMTS13の検査結果が手元に届くまでは通常数日以上かかることに注意です.
便培養では病原菌の検出はありませんでした.
よってTTP,STEC-HUSの可能性は低く,aHUSの可能性は残っています.
症例提示の際,みなさんには病歴・症候・初回の検査結果をふまえて,初期治療の内容を回答いただきました.みなさんの回答は以下です.
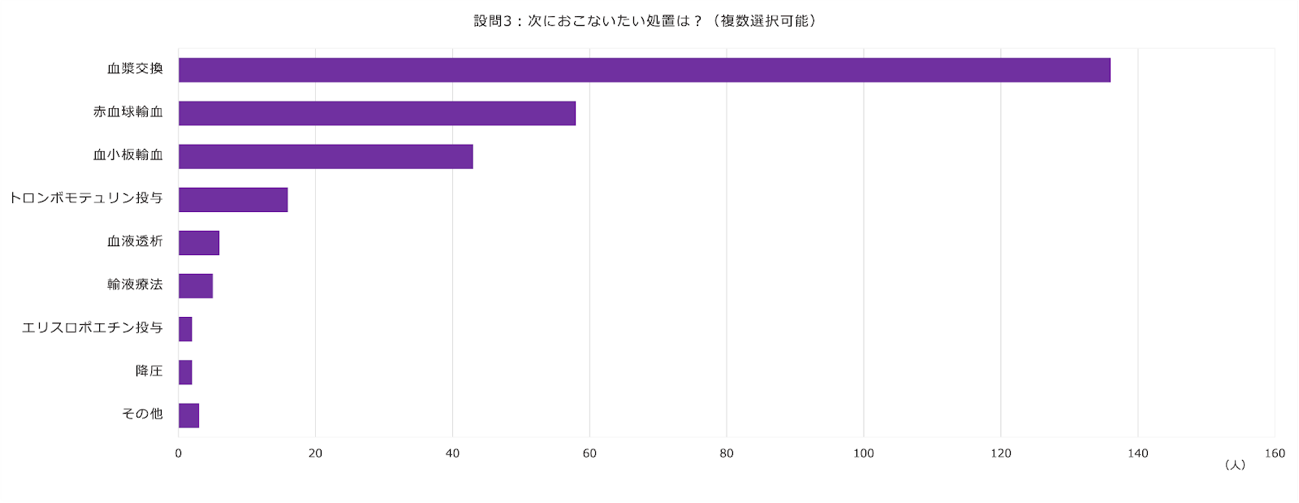
最も多い回答は血漿交換です.TTPは血漿交換なしでは最大90%が死に至ります [4]が,適切に血漿交換を導入すれば死亡率を20%未満に低減できます[2].
ひとたびTTPを疑えば,4~8時間以内に血漿交換をおこなうべき[2]である一方でTTP診断に必要なADAMTS13の結果が到着するには数日以上かかります.
TTPらしいかどうかはPLASMICスコア(表3)が参考になります[5].本症例のスコアは5点で中リスクであり,TTPである確率は9~24%と見積もられます[5].
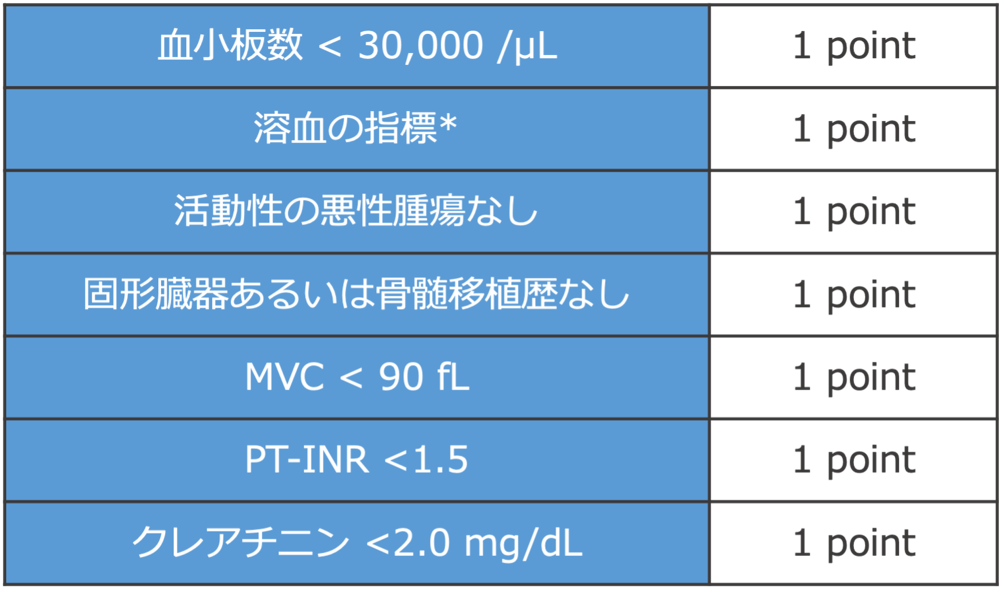
表3. PLASMICスコア(TTPの予測スコア)
0-4point: 低リスク 5point: 中リスク 6-7point: 高リスク
*網赤血球>2.5%あるいはハプトグロビン検出感度以下あるいは間接ビリルビン>2.0mg/dL
TTPの死亡率に対して血漿交換の治療効果が大きいことを考えると,TMAの病型が明らかになるまでは血漿交換をおこなうという方針は許容されます.
さらにaHUSや薬剤性TMAなど,TTP以外のTMAでも血漿交換の効果は報告されています.
次に輸血について注意点です.出血を合併していないTMA患者への予防的血小板輸血は,血栓症を増悪させるため原則禁忌であることは覚えておきましょう.過剰な血小板凝集に,さらに燃料を投下することになり,fuel on the fireと表現されます.
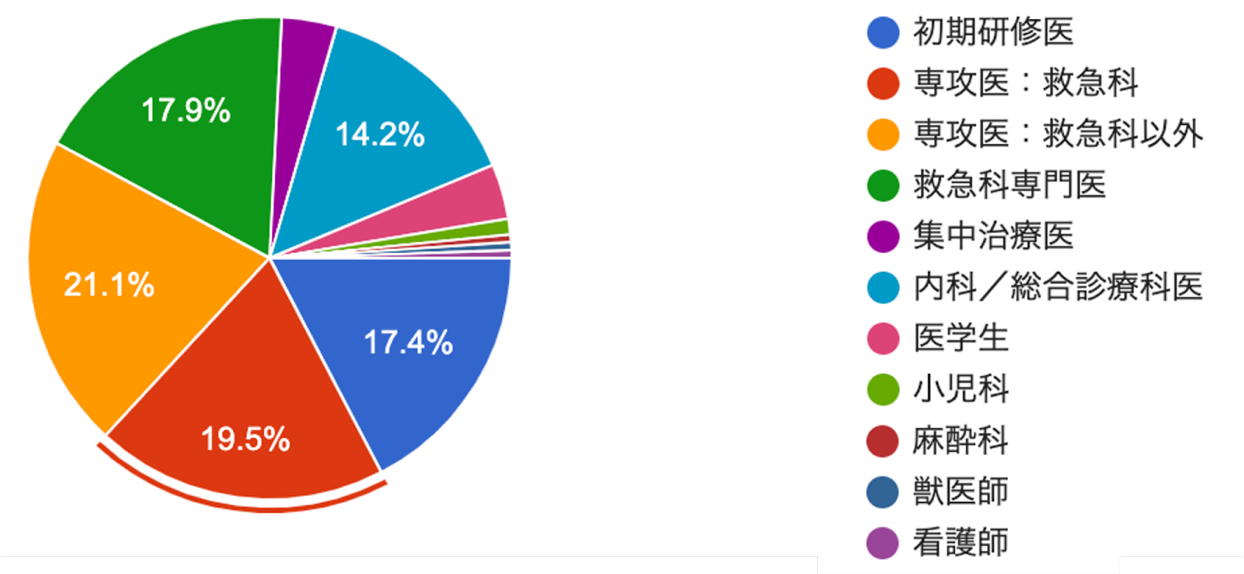
設問に答えてくださった合計198人の方々,ありがとうございました!回答者は以下のような内訳でした.
本症例のその後の経過
まず我々は来院日の血液検査データから何らかのTMAを疑いました.初期治療は,血漿交換,血液透析を併用した体液管理,プレドニゾロン60mg内服です.血小板輸血はせず,赤血球輸血もまずはおこないませんでした.
治療経過は良好で,血漿交換を6コースおこないました.第6病日にADAMTS13活性が正常であることが分かりTTPが否定されました.血漿交換離脱後の第9病日のデータは表4です.
血小板増加,腎障害軽減,溶血軽減を認め,全体的として大きく改善しました.
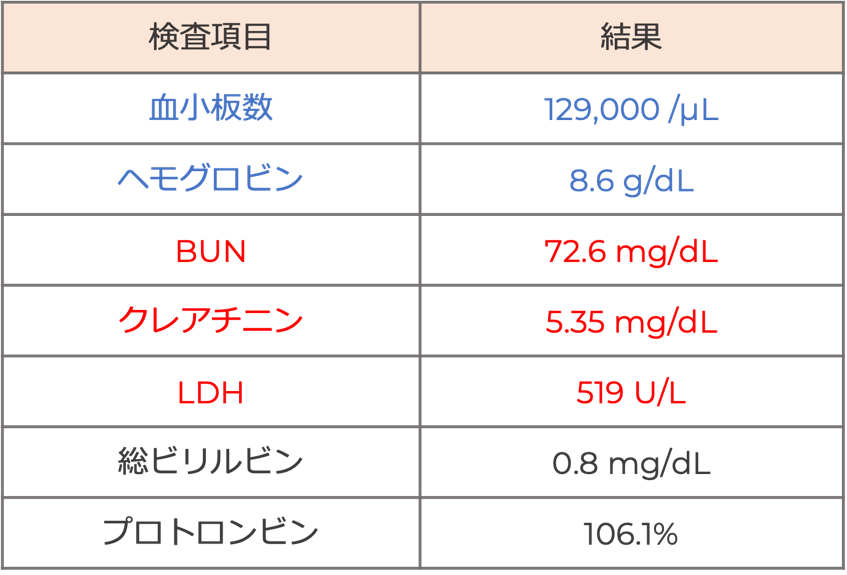
表4. 血漿交換後の検査結果
aHUSを疑い遺伝子検査をおこなったところCFH遺伝子変異が検出されました.aHUSと確定診断,ラブリズマブを投与し,第40病日に退院しました. ステージ5の重度な慢性腎臓病は残存したものの,血液透析は離脱できました.
補体介在性HUS
aHUSは,従来STEC-HUS以外のHUSのことを示していました.しかし現在は病態理解が進み,補体介在性HUS (CM-HUS) と呼ばれることが多い疾病です.aHUSの認知度が高くはありますが,本稿でも以降は病態に即してCM-HUSと呼びます.
CM-HUSは補体の第2経路の異常な活性化に起因[2]し,多くは遺伝的異常が関連していますが,60%は成人発症です[2].
CM-HUSの予後は悪く,死亡率は9-25%とされ[6],発見し治療につなげることが非常に意義のある疾患です.
症状は臓器横断的で,ある報告によれば,代表的な症状は以下の通りです[6].
・ 消化器症状(下痢・腹痛):51%
・ 神経症状(頭痛・意識障害など):49%
・ 発熱:17%
また血圧は高値を示すことが多く,同報告では血圧の中央値は150/80 mmHgでした[6].
本症例も消化器症状を主訴として来院され,高血圧を有していましたね.
CM-HUSの診断は一般的に容易ではありません.短期間でCM-HUSを直接的に診断する方法は存在しないからです.
補体関連の遺伝子検査は特殊であり,CM-HUSを強く疑わない限り,検査されることはありません.検査結果の到着まで,週単位で時間がかかることもあります.
信頼できる決定的な検査がないことから,CM-HUSは通常,他のTMAとDICを除外することで診断につながります[3].
実際に,救急外来で血小板減少を見つけたときCM-HUSを見逃さないための診療手順を説明します.
まずは,既往歴に原因がはっきりしない腎障害や脳血管障害がないかをチェックしましょう.本症例では健康診断で尿潜血の指摘がありました.
同様に腎障害や脳血管障害の家族歴をチェックします.CM-HUSの概念が広がったのは最近であり,原因不詳の重症病態の家族歴は,実はCM-HUSであった可能性があります.
なお,本症例は家族歴はありませんでした.遺伝は不完全浸透であり,有意な家族歴がないことも多くあります.
検査学的には図2のフローのように精査を進めますが,救急外来レベルではTMAと診断するところまでが限界で,TMAの病型診断は不可能です.
設問1で多くの方が挙げてくださった,HUSとTTPは,いずれもTMAの病型の一つで,設問1の初診時点では,診断できません.
CM-HUSやTTPは感染症を契機に発症し,一見して敗血症性DICと区別がつかない症候やデータになることもあり,TMAと気づかない可能性も十分にあります[3].TMAはDICと診断される可能性が高く,適切な治療が遅れてしまう可能性が懸念されています[1].
つまり初診時に疑うだけでなく,感染症治療をしてもよくならない血小板減少,腎障害はCM-HUSを疑う手がかりになります.
なおC3 低値かつ C4 正常値は補体の第二経路の活性化が示唆されCM-HUSを強く疑う所見です[2].しかしC3 低下例は約半数程度であり[2],血清補体価はCM-HUSの参考所見です.
治療は抗補体抗体でエクリズマブ(ソリリス®︎)が長く使われてきましたが,2020年にラブリズマブ(ユルトミリス®︎)が承認されたことはトピックです.エクリズマブは2週間,ラブラリズマブは8週間隔で投与を続けます.
これらの薬剤は髄膜炎菌感染症のリスクを著しく増大させることに注意しましょう.利用にあたり髄膜炎菌ワクチンの接種が必要です.それでも抗補体抗体薬の利用者が救急外来に来たら,髄膜炎菌感染症を鑑別に入れることは非常に大切なことです.
さらにCM-HUSに対し,血漿交換は一定の効果が報告されています[2, 7].TMAの病型を判断しながら,血漿交換をはじめておくというのは,TTP治療だけでなくCM-HUS治療としても妥当性があるでしょう.
Take home message
1. 血小板減少+凝固障害なし+溶血性貧血あり→微小血管障害症 (TMA)を考えよう
2. 感染症に合併する血小板減少は播種性血管内凝固症候群 (DIC)だけではない
3. 感染治療をしてもよくならないDICでは、TMAの可能性を思い出そう
いかがでしたでしょうか.TMAは多様な病態を内包しており,苦手意識がある方も多いのではないでしょうか.Take home messageをおさえることで,複雑なTMA診療が単純化されるはずです.本稿が,みなさんの明日からの診療に少しでも役立つことを祈ります.
引用文献
[1] Vincent JL, Castro P, Hunt BJ, Jörres A, Praga M, Rojas-Suarez J, et al. Thrombocytopenia in the ICU: disseminated intravascular coagulation and thrombotic microangiopathies-what intensivists need to know. Crit Care. 2018;22(1):158.
[2] 香美 祥二, 岡田 浩一, 南学 正臣, 要 伸也, 丸山 彰一, 安田 隆ら. 非典型溶血性尿毒症症候群(aHUS)診療ガイド2015. 日本腎臓学会誌. 2016;58(2):62-75.
[3] Iba T, Watanabe E, Umemura Y, Wada T, Hayashida K, Kushimoto S, et al. Sepsis-associated disseminated intravascular coagulation and its differential diagnoses. J Intensive Care Med. 2019;7:32.
[4] Rock GA, Shumak KH, Buskard NA, Blanchette VS, Kelton JG, Nair RC, et al. Comparison of plasma exchange with plasma infusion in the treatment of thrombotic thrombocytopenic purpura. Canadian Apheresis Study Group. N Engl J Med. 1991;325(6):393–7.
[5] Bendapudi PK, Hurwitz S, Fry A, Marques MB, Waldo SW, Li A, et al. Derivation and external validation of the PLASMIC score for rapid assessment of adults with thrombotic microangiopathies: a cohort study. Lancet Haematol. 2017;4(4):e157–64.
[6] Jamme M, Raimbourg Q, Chauveau D, Seguin A, Presne C, Perez P, et al. Predictive features of chronic kidney disease in atypical haemolytic uremic syndrome. PLoS One. 2017;12(5):e0177894.
[7] Noris M, Caprioli J, Bresin E, Mossali C, Pianetti G, Gamba S, et al. Relative role of genetic complement abnormalities in sporadic and familial aHUS and their impact on clinical phenotype. Clin J Am Soc Nephrol. 2010;5(10):1844–59.