EMA症例130:2月症例解説
2月症例の解説編です。今月は約280名の方にご回答頂きました。みなさまご参加ありがとうございました!
<設問4:属性(職種)について>
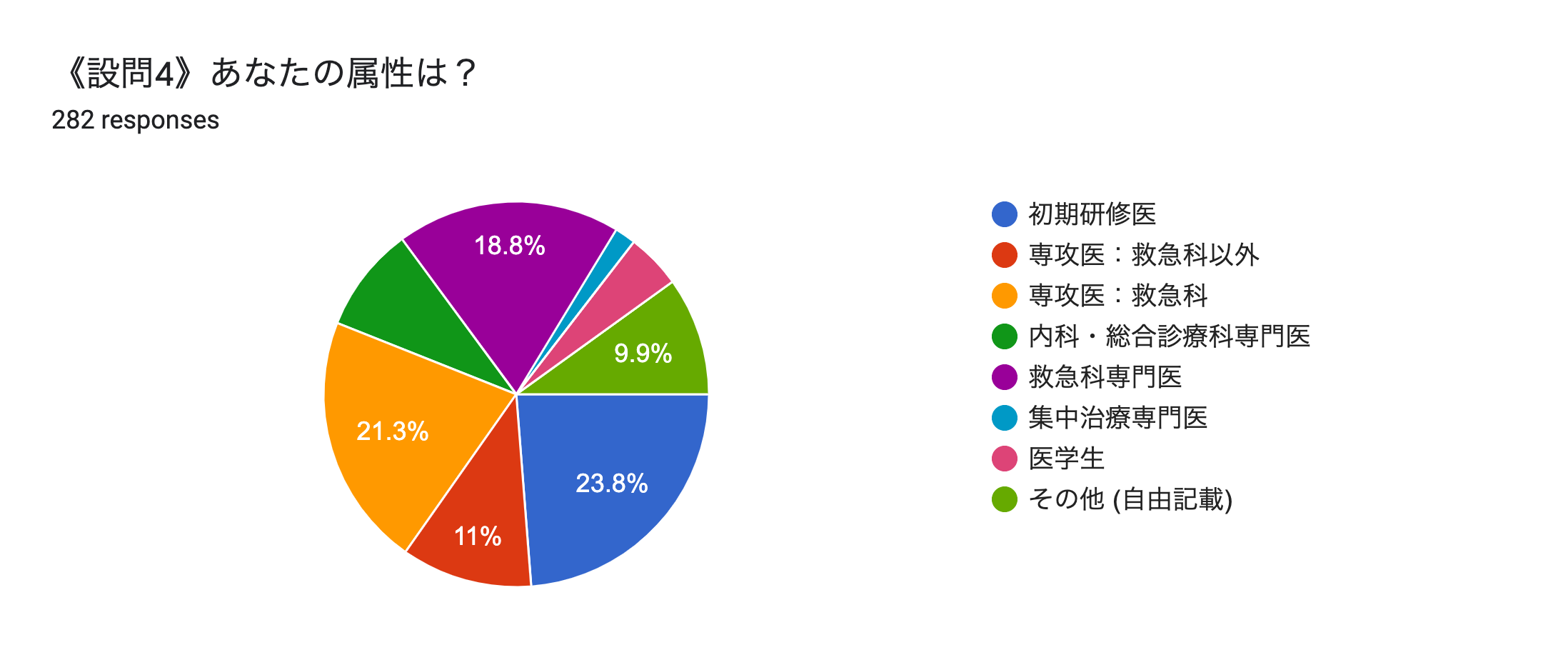
初期研修医:67(23.8%) 専攻医(救急科以外):31(11%) 専攻医(救急科):60(21.3%) 内科・総合診療科専門医:25(8.9%) 救急専門医:53(18.8%) 集中治療専門医:5(1.8%) 医学生13(4.6%) その他:28(9.9%)
今回は、意識障害で搬送された患者さんの症例でした。左共同偏視があるということで、脳卒中やてんかんが頭に浮かびますが、まずは血糖値をチェックすると思います。血圧が113/61mmHgと高くないことからは、「頭以外」の原因を積極的に探す必要がありそうな第一印象を持ちながら、既往からは原病や薬剤の関与もありそう…などと考えながら診療を進めるのではないでしょうか。
結果的に、提示した検査結果では、血清Na99mEq/Lという著明な低Na血症が目立ちますね。血液ガスからすぐに診断はつきましたが、さて、原因は何だろう、治療はどうするんだっけ。ということで、今回は低Na血症の「マネジメント」に焦点を当てたいと思います。
■ 低Na血症
低Na血症の定義は血清Na<135mmol/Lで、血清Na130-134mmol/Lを軽度、血清Na 125-129mmol/Lを中等度、血清Na<125mmol/Lを重度の低Na血症と分類します。低Na血症は、救急外来で遭遇する最も多い電解質異常のうちのひとつです(1)。しかし皆さんもご存知の通り、その多くは緊急での介入を要しません。しかしながら、入院患者において軽度(血清Na130-134mmol/L)の低Na血症であっても入院後の死亡率の増加と関連していたという報告があり(2)、低Na血症の重要性が注目されています。また、救急外来では重症低Na血症に対して緊急の治療を要する場合が必ずあります。そこで今回は、低Na血症のマネジメントについてまとめてみました。
■ 低Na血症の診断アルゴリズム
ヨーロッパ集中治療医学会(ESICM)、ヨーロッパ内分泌学会 (ESE)、ヨーロッパ腎臓学会・透析移植学会 (ERA-EDTA)の3学会は、合同で低Na血症のガイドライン(以下、欧州ガイドライン)を作成し、2014年に発表しました(3)-(5)。欧州ガイドラインで示された低Na血症の診断アルゴリズムを示します(図1)。特徴としては、アルゴリズムの上流では細胞外液量(Extracellular fluid)を評価せず、尿浸透圧や尿Na濃度に基づいて診断を行う点です。
このアルゴリズムの背景としては、細胞外液量を臨床的に評価する指標が乏しいことや、細胞外液量の評価が上流にあるアルゴリズムを使用した場合の診断の的中率は、わずか10%程度であったという報告があります(6)。一方で、尿浸透圧や尿Na濃度に基づいた診断アルゴリズムを使用した研修医のグループは、アルゴリズムを用いない集中治療医のグループよりも、低Na血症の原因診断における的中率が高かったという報告もあります(7)。救急外来では限られた情報と時間の中で低Na血症の原因を検索する必要があり、尿浸透圧や尿Na濃度に基づいた診断アルゴリズムが使いやすいかと思います。
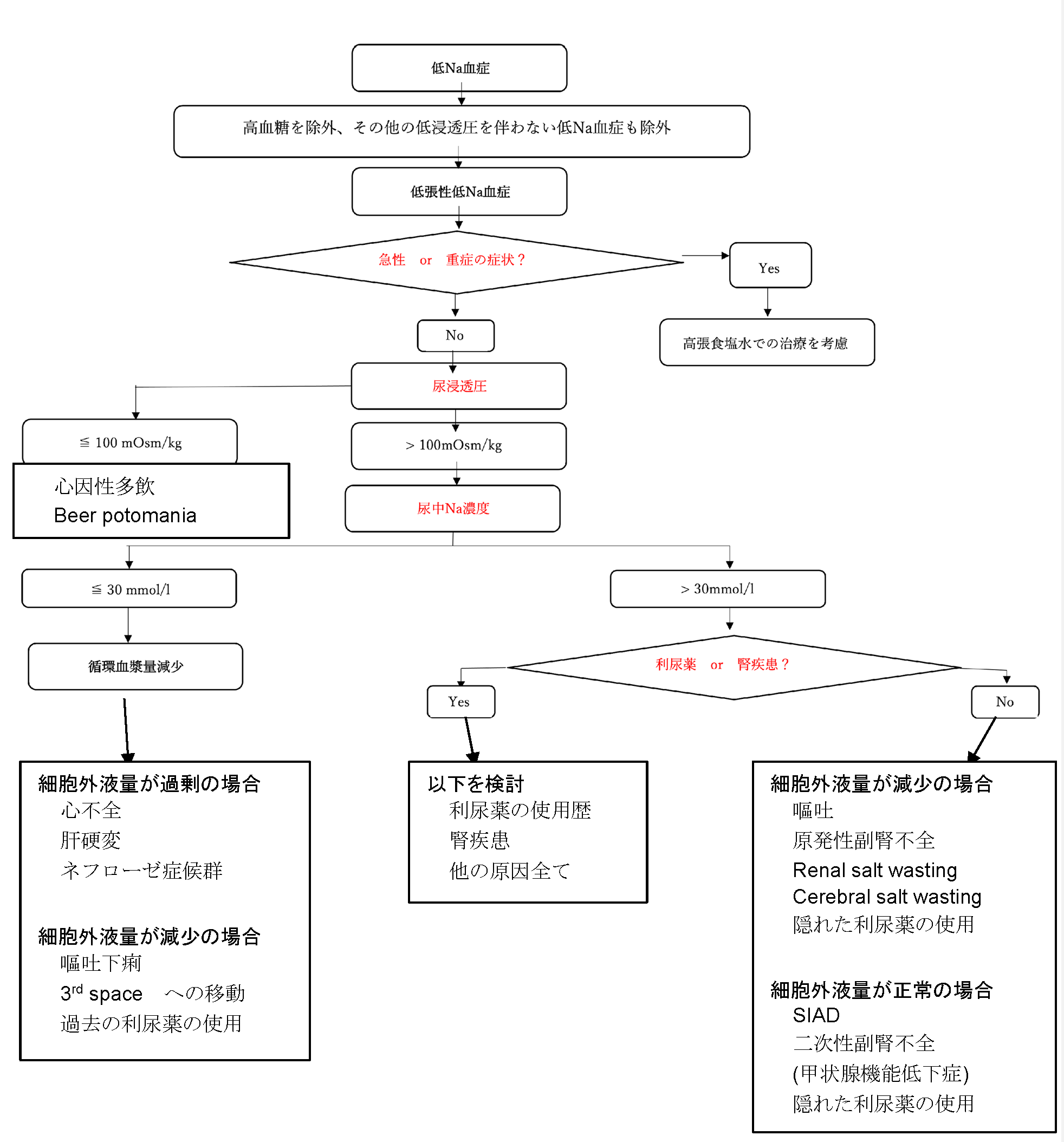
図1:低Na血症の診断アルゴリズム(文献(3)-(5)から改変)
ここで、設問1に対するみなさんの回答を発表します。
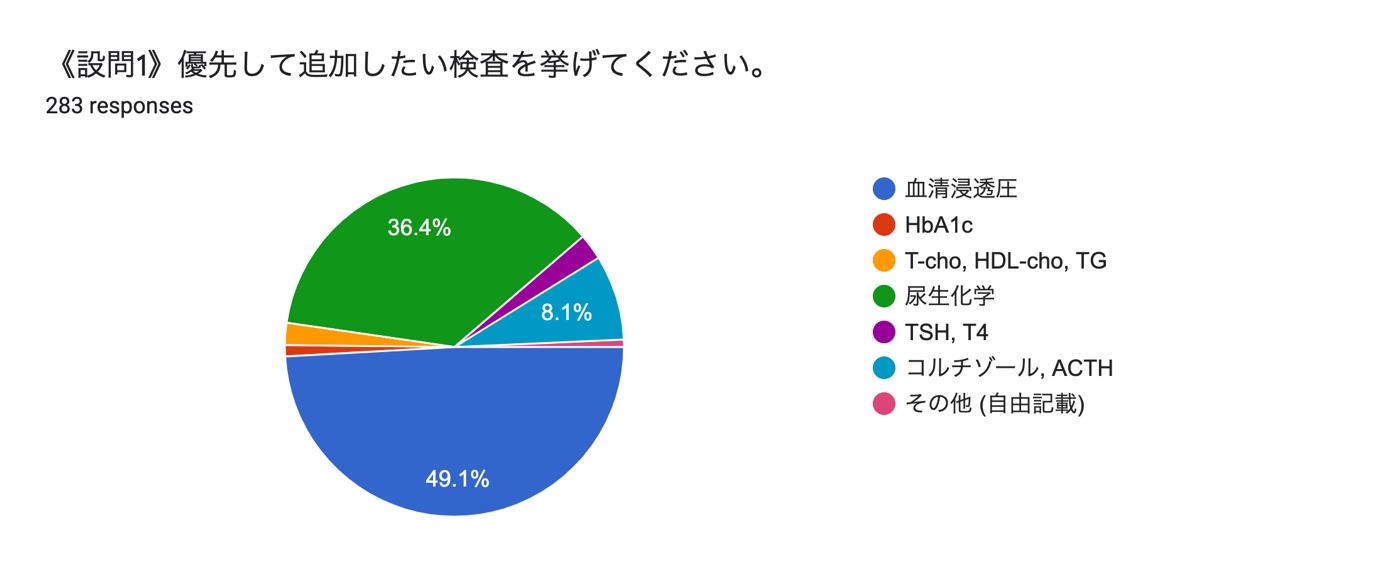
低Na血症の鑑別に必要な検査を選んでいただけたと思います。アルゴリズム通り、まず偽性低Na血症を否定し原因検索をするという気持ちで検査を選んでいただいた方が多かったように思います。治療の方向性に大きく影響しますので、利尿薬の使用や心不全の既往などの病歴聴取も大切です。また、低Na血症を見たら、原発性副腎不全や甲状腺機能低下症はないか、追加の血液検査を行い鑑別しましょう。原発性副腎不全の診断ではACTH負荷試験がゴールドスタンダードですが、救急外来ではランダムコルチゾール検査が現実的です。ACTH負荷試験と血清ランダムコルチゾール値の関係を調べた報告から、ランダムコルチゾール>15.2μg/Lでは副腎不全がほぼ否定できることがわかっていますので(8)、救急外来でのコルチゾール値が低くなければ副腎不全は否定的と言えます。一方、甲状腺機能低下症に関しては、粘液水腫性昏睡のような重症の場合を除いて甲状腺機能低下症が低Naの原因であることはまれであることが報告されており(9)(10)、欧州アルゴリズムのガイドラインでも括弧付きで表記されています。低Na血症の患者で甲状腺機能低下症が見つかったとしても、他に原因がないか慎重な検索が必要であると言えます。
■ 体内水分量の調節
低Na血症の病態は、体内のNa量調節の異常ではなく体内の水分量の調節の異常であると解釈されています。体内の自由水のバランスは視床下部にある浸透圧受容体で感知されています。この受容体は鋭敏で、セットポイントである280mOsm/kgから3mOsm/kgのズレを感知できるとされています(11)。体内の自由水が上昇したとき、それに伴う細胞外液浸透圧の低下に反応し、バソプレシン分泌が抑制され、アクアポリン2受容体の調節を介して腎での自由水再吸収が抑制されます。浸透圧低下の信号は、これと並行して口渇中枢に伝わり、口渇が抑えられ、自由水摂取が抑制されます。この二つの経路で、体内の自由水増加による浸透圧低下が調整されます。
それでは、アルゴリズムを上流から順番にみてゆきましょう。
■ 偽性低Na血症
まずは浸透圧を確認し、偽性低Na血症や等張性低Na血症を除外します。偽性低ナトリウム血症は、脂質やタンパクが異常高値の際(総コレステロール>977 mg/dL、総タンパク>10g/dLなど(12))に起こりえます。検査室では血液を希釈して生化学検査を行っています。図2に示すように、検体Aと検体Bという、ブルーの液相には同じNa濃度、同じ浸透圧の検体があるとします。ピンク色の固体相に含まれるのは脂質やタンパク質です。固体相が異常に多く含まれる検体Bの場合、相対的に液相の容量が少ないですが、検体Aにも検体Bにも同量の液体が加えられ希釈されます。その結果、検体Aと検体BのNa濃度は同じはずだったのに、検体Aは正常、検体Bは低Naとして報告されます(3)-(5)。
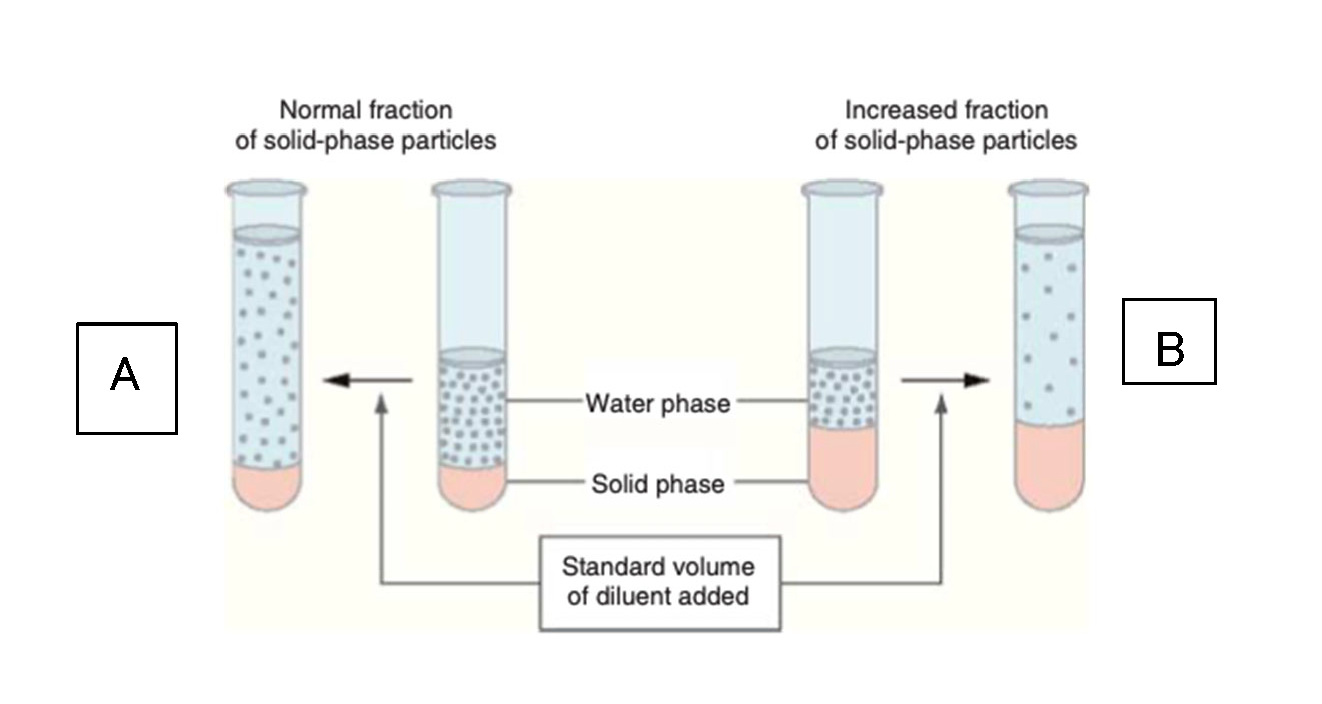
図2:偽性低Na血症のメカニズム(文献(3)-(5)より改変)
高血糖の時の偽性低Na血症はこれとは異なる機序で起こります。細胞膜を自由に行き来しないために張力を発生し細胞内外の水の移動に関与する物質を有効浸透圧物質といい、Na、血糖、マンニトールなどがあります。高血糖の条件では、細胞外液の血糖が直ちに細胞内に取り込まれず細胞内外に浸透圧差が生じ、細胞内から細胞外に自由水が移動し、その結果、等張性低Na血症となります(13)。
■ 急性か慢性か?
急性低Na血症は48時間以内に発症したものを、慢性低Na血症は48時間を超えて持続する低Na血症を指します。急性の場合は症状を呈しやすいと言われますが、急性か慢性かについては病歴から探る必要があります。慢性の経過で低Na血症を生じた場合、脳細胞内からNaやK、その他有機溶質(ミオイノシトールなど)が排出され、細胞外液の浸透圧低下に合わせて脳細胞内の浸透圧も低下させるという適応(regulatory volume decrease) が起こります(11)(14)。脳細胞が低浸透圧に”適応”した状態で、低Na血症の治療により細胞外液の浸透圧が急速に上昇した場合、細胞外の電解質は数時間で細胞内に移動しますが、有機溶質が移動するには1週間程度かかると言われています。そのため急激に細胞外液のNa濃度を補正すると、細胞内外での浸透圧ギャップが生じ、浸透圧性脱髄が起こると考えられています。
■浸透圧性脱髄症候群
以前、橋延髄脱髄症候群とよばれていた病態は、浸透圧性脱髄症候群という用語に統一されています。理由としては、橋のみに病変がある症例の割合は56%程度で、橋以外にも病変があることが多いためです(14)(15)。病変の位置に応じて意識障害、球麻痺(構音障害、嚥下障害)、四肢麻痺やパーキンソン様症状(四肢固縮、動作緩慢、振戦)を生じます(13)。浸透圧性脱髄症候群の症状は、低Na血症の補正後3-15日後に生じます(15)。つまり、いったん低Na血症による症状が消失し、再度症状が悪化したように見えることがあります。浸透圧性脱髄症候群を発生させない観点からは、低Naの発症が急性か慢性かわからない時は、慢性として治療を開始することが推奨されます(3)-(5)。
ところで、浸透圧性脱髄症候群の予後に関しては、これまでは非常に悪いと考えられてきました。しかし、近年の36人のICU症例の報告では、治療開始時の重症度と長期予後にあまり差がないことや、最初の症状が重症であったために治療の差し控えがされた患者の中にもRankin scale ≦1まで回復した症例があったことなどが報告されており、発症時の症状から長期予後を予測できないと結論されています(16)。
■ 重症の症状とは?
欧州ガイドラインでは低Na血症の症状を以下のように分類しています。
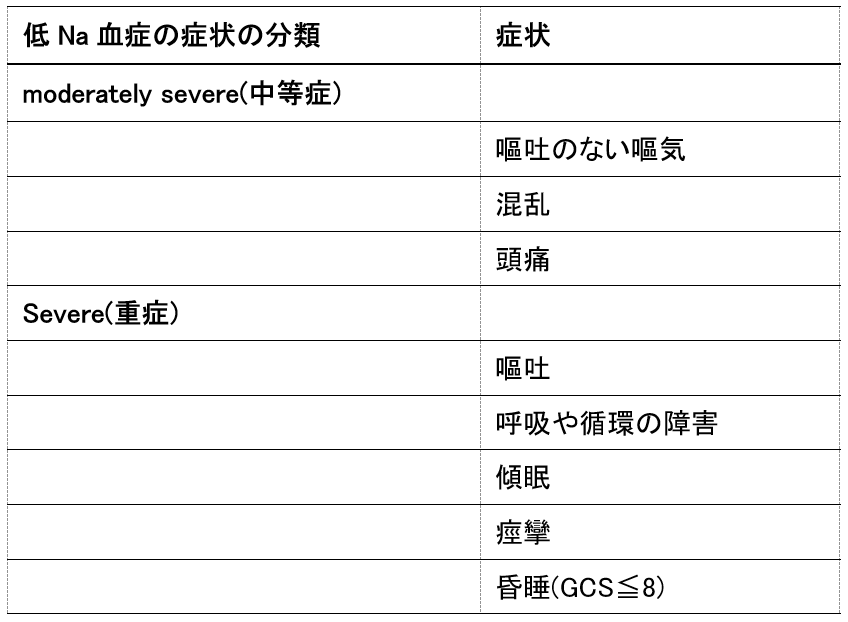
表1:低Na血症の症状の分類
■ 本症例の低Na血症の病型は?
本症例について、フローチャートに沿って考えてみます。まず、血清浸透圧は205mOsm/Lであり低張性低Na血症であると確認できました。次に症状を確認しますが、本症例では痙攣と傾眠があり重症の症状を伴う重度の低Na血症と言えます。
ここで、設問2に対するみなさんの回答を発表します。
<設問2:低Na血症の原因として何を想定しますか?>
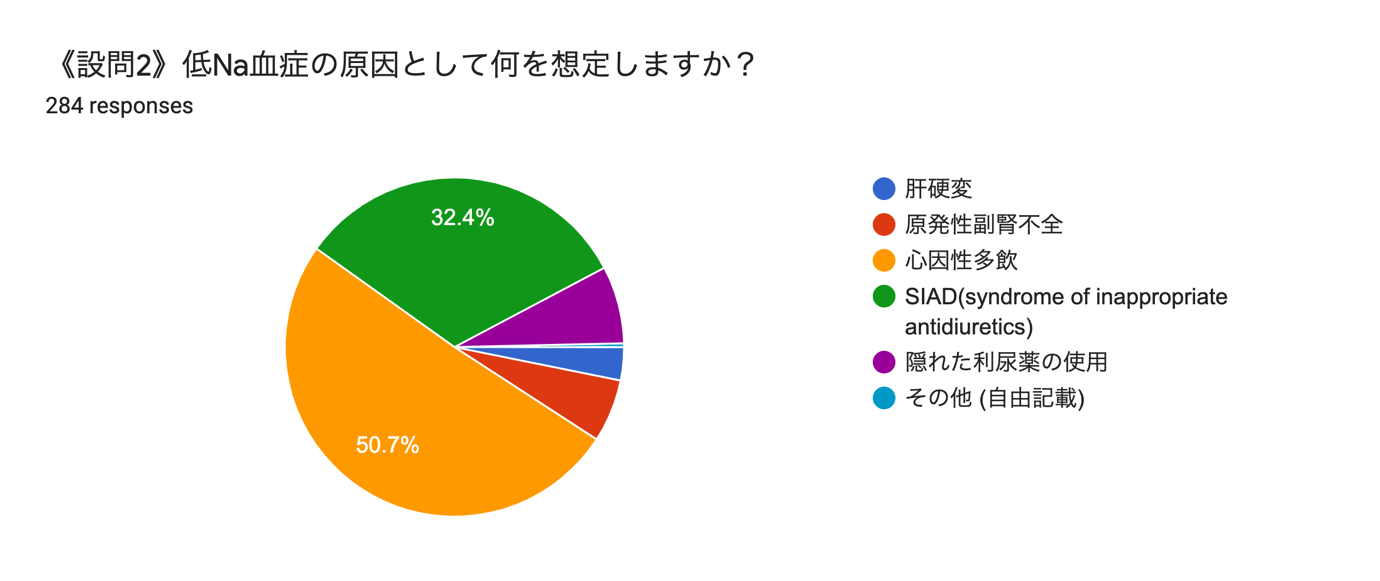
<設問3:どのように治療を開始しますか?>
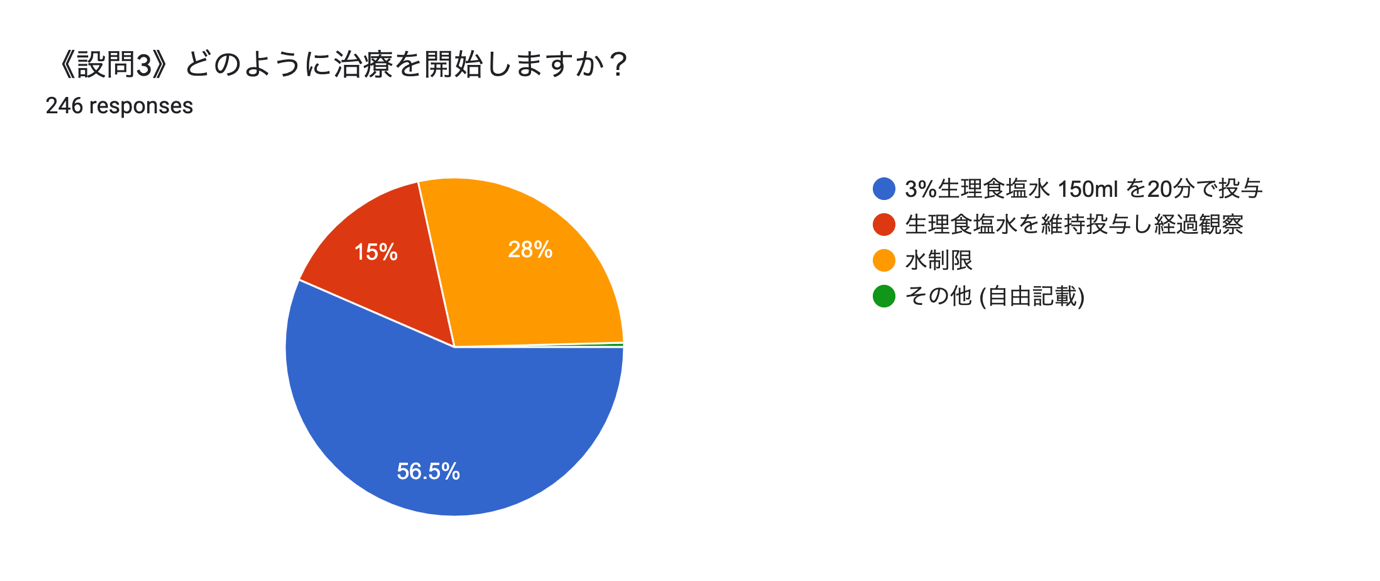
設問3では、ほとんどの方が高張食塩水を挙げておられました。重症の症状があることからアルゴリズムに従うと、適応があると思われます。しかし、高張食塩水を使用したらあっという間に過補正になってしまい、脳浮腫よりも浸透圧性脱髄症候群の方が心配になってしまった、という経験はないでしょうか?今回、高張食塩水以外の選択肢を選んだ方の中には、過補正への配慮をされた方もいらっしゃると思います。
■ 重症の症状がある低Na血症
そもそも低Na血症は、どのくらい急いで治療したほうが良いのでしょうか?この問いに正確に答えることは難しいですが、重症の症状を伴う低Na血症の患者さんでは脳浮腫をきたしていると考えられ、後遺症や脳ヘルニアを防ぐため、速やかな補正が望ましいとされます。欧州ガイドラインでは3%食塩水150mlまたは2ml/kgを20分での投与が推奨されています。少量持続静注と急速ボーラスの反復では、過補正のリスクは変わらないが、ボーラスの方が過補正に対する逆補正が少なかったという一つのRCTもあり(16)、投与の仕方はどちらでも良いと思いますが、手順としてはボーラスの方がシンプルかと思います。最初の目標は血清Naの5mmol/L上昇です。5mmol/Lの上昇で症状が改善することが多いためです。改善しない場合は血清Naが10mmol/L上昇、または血清Naが130mmol/Lとなるまで3%食塩水150mlを反復投与します。全体の補正の速度は最初の24時間で10mmol/L、その後は8mmol/L/日までに制限します(3)-(5)。
■Edelmanの式とAdrogue-Madiasの式
1985年Edelmanは、体内Naイオン量と体内Kイオン量の関係を以下のように示しました。
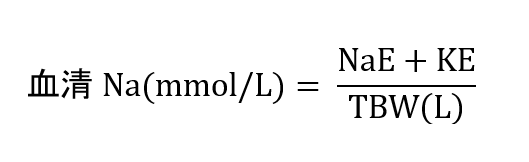
NaE:体内のNaのうち交換可能な(骨などを構成していない)Naで約70%とされる
KE:体内のKのうち交換可能なKで約85%をしめる
TBW:体内総水分量(L)
男性:0.6×体重(kg)、女性:0.5×体重(kg)
体内のNaの70%が交換可能なNaでほとんど細胞外液に存在し、残りの交換不可能なNaは骨に含まれています(13)。同様に体内のKの85%が交換可能なKで細胞内に存在します(11)。臨床で問題になるのは交換可能なNaとKのことであるので、NaEとKEは血清Naと血清Kに置き換えて解釈可能です(11)。この式からは血清Na値は血清Kに影響を受けることがわかります。これは細胞内からKが細胞内に移動した場合、その分同じ陽イオンであるNaが細胞内に移動し血清Na値は下がるので、血清Kは血清Naに大きく影響すると考えられています(13)。この式からは、尿中(Na+K)が血清Naと同じであれば、血清Naは変化しないことがわかります。一方で、尿中(Na+K)が血清Naより低ければ、血清Naは上昇すると予想できます。
Edelmanの式から導かれるAdrogue-Madiasの式は、輸液に対する血清Naの上昇の予測に一般的に使用されます。補正速度のコントロールに活用できる可能性はありますが、この式は、輸液が投与されるが体内では何もおこらないことを前提としているため、理論的には無尿の時に成り立ち、希釈尿が大量に出ている場合は過補正となってしまうことに注意が必要です(18)。予測式には限界があることから、採血フォローアップが最も重要とも言えます(19)。
1Lの補液をしたときの血清Naの変化
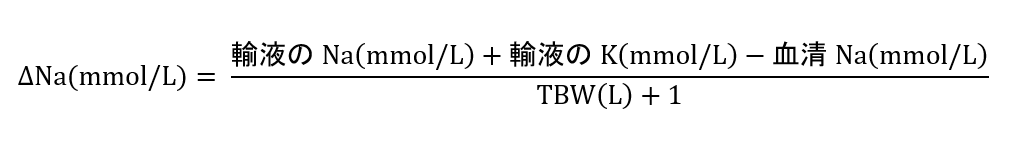
ΔNa:輸液投与後の血清Naの濃度変化
TBW:体内総水分量(L)
男性:0.6×体重(kg)、女性:0.5×体重(kg)
<<症例の経過>>
本症例は高張食塩水投与が考慮される症例でしたが、アルゴリズムをさらに進めてみると、尿浸透圧は188mOsm/L>100mOsm/L、尿中Naが27mmol/L< 30mmol/Lですが、嘔吐や利尿薬使用の病歴はなく、副腎不全も否定的で、SIADは鑑別として残るものの明らかな原因が不明でした。その他の原因も考慮しましたが、心不全や肝硬変、ネフローゼなど有効循環血液量の低下を伴う病態とは合致しそうではありませんでした。尿中Naが低くない事は合いませんが、統合失調症の既往からは水中毒は想起されました。尿道留置カテーテルからは2時間で2400mlの大量の希釈尿を認めていました。
尿中Na(27 mmol/L)+尿中K(13.6mmol/L) = 40.6mmol/L < 血清Na(99mmol/L)
上記からは尿から自由水が排泄されている状態と考えられますので、水制限のみで自然に血清Naが回復する可能性は高いと考えました。そこでまず生理食塩水を100ml/hで投与しながら、意識障害の原因検索としての頭部CT検査などを実施しました。その結果2時間で104mmol/L(Δ5mmol/L)まで血清Naが上昇しました。しかし、傾眠状態(E3V1M4)の改善はなく大腿四頭筋などで筋攣縮が頻発していました。そこで3%食塩水を使用する方針とし、100ml(2ml/kg)を投与しました。3%食塩水は100mlに3gのNaClが溶解している食塩水のことですので、1molのNaClは58.4gであることから計算すると、3%食塩水は3÷58.4×10×1000=513.7mmol/Lです。みためは体重50kg程度のやや痩せ型の男性でしたので、TBW=0.6×体重(kg)=3(L)と推定しました。
Adrogue-Madiasの式に代入すると、

となります。今回は補液は1Lではなく100mlですのでΔNaは1.32mmol/Lと予想されます。尿量が保たれていたので予測式以上の補正が見込まれましたが、結果としては血清Naは105mmol/L(Δ1mmol/L)までの上昇にとどまりました。尿量は保たれたままでしたので、生理食塩水10ml/hを継続としてこれ以上の積極的なNa補正はしないこととし、1時間毎に採血フォローを予定しました。この時点で補液のためかSpO2がやや低下したこともあり、遷延する意識障害に対する気道の確保目的に、プロポフォールを用いて鎮静し、挿管管理の方針としました。挿管となると症状改善の確認ができませんので、最初の24時間で血清Na10mmol/Lまでの上昇を目標としました。当院がベッド満床であったためこの方は他院へ転院となりました。
■水中毒
水中毒は、腎臓が希釈できる限界の量を超えた自由水が摂取されることにより起こります。治療は水制限です。ただし、以下の場合には水制限に反応しないことが予想できます。

表2:水制限不応の予測因子
文献(11)より改変
低Na血症の治療において、低Na血症の悪化は避けたいですが、SIADのように尿の浸透圧が上昇している病態でも、理論的には3%を超えた濃度の尿を生成できないので、3%食塩水を使用すれば低Na血症が悪化することはありません。そこで、積極的なNa負荷には3%食塩水が選択されています(13)。
■ 浸透圧性脱髄症候群のリスク因子
症例対照研究の結果などから以下が示唆されています。

表3:浸透圧性脱髄症候群のリスク因子
文献(15)より改変
■ 過補正となってしまった際の逆補正
過補正となった場合の逆補正として、欧州ガイドラインの推奨では、積極的なNaの投与を止めること、自由水を10ml/kg/hで投与すること、デスモプレシン2μgの投与を考慮することがあげられています。また、desmopressin acetate (DDAVP) clampと呼ばれる、3%食塩水と同時にデスモプレシン2μg 8h毎を投与する方法が2013年に紹介されています(20)。高張食塩水を使用して低Na血症を治療している最中に、低Na血症となった原因が改善し、ADH分泌が低下することで急速に水利尿が起こり、血清Naが急上昇してしまう場合があります。Naの投与と同時にデスモプレシンを投与しておけば、そのような急速な変化を起こさずコントロールできるということになります。
■過補正となりやすい低Na血症
過補正となりやすい低Na血症の病態を意識しておくことも、過補正の予防に役立ちます。過補正となりやすい状況を、以下の表にまとめました。

表4:過補正となりやすい低Na血症
文献(15)より
■ 抗精神病薬内服と水中毒
統合失調症患者の低Na血症は複合的な原因で起こります。抗精神病薬の副作用には口渇を生じるものが多く、また統合失調症の症状としての心因性多飲の要素が加わって、患者が自由水を大量摂取することにより、いわゆる水中毒となります。しかし、精神科薬剤の副作用によるSIADも低Na血症の発症に寄与しており、その影響で、尿浸透圧>血清浸透圧の場合が多いという報告もあります(21)。本症例では希釈尿が出ていたにもかかわらず血清Naの補正は比較的緩やかで、自由水の大量摂取以外にも低Na血症の原因があることが予想されました。このように、アルゴリズムに基づいた診断が臨床状況と合わない場合や、診断に基づいた治療を開始しても低Na血症が改善しない場合は”unresolved hyponatremia”として再評価が必要であり、“専門科へのコンサルト”という選択肢も推奨となります(3)-(5)。今回の症例は、心因性多飲+SIADの両方の病態の併存と考えました。
<<症例の経過>>
本症例は、ベッドが満床であったため転院となりました。転院先のICUで順調にNaは補正され抜管もできたとのことでした。
■ おわりに
低Na血症の治療は救急外来では完結しませんが、救急外来でベストなNa補正を開始することが求められます。特に、重症の症状のある低Na血症は脳浮腫を反映しており、浸透圧性脱髄症候群のリスクを考慮しながらも短時間での補正が必要です。患者さんの良好な予後を目指し、救急外来での良い塩梅を探しましょう。
■ Take Home Message
・低Na血症の原因検索にはアルゴリズムの使用が勧められるが、当てはまらない場合もある
・重症の有症状の低Na血症の治療はまず3%食塩水150mlまたは2ml/kg
・過補正になりやすい低Na血症の原因を認識し注意する
・浸透圧性脱髄症候群の予後は以前考えられていたよりも良好である可能性がある
■ 参考文献・資料
1.Imai N, Osako K, Kaneshiro N, Shibagaki Y. Seasonal prevalence of hyponatremia in the emergency department: impact of age. BMC Emerg Med. 2018;18(1):41. Published 2018 Nov 15. doi:10.1186/s12873-018-0182-5
2.Waikar SS, Mount DB, Curhan GC. Mortality after hospitalization with mild, moderate, and severe hyponatremia. Am J Med. 2009;122(9):857-865. doi:10.1016/j.amjmed.2009.01.027
3.Spasovski G, Vanholder R, Allolio B, et al. Clinical practice guideline on diagnosis and treatment of hyponatraemia [published correction appears in Intensive Care Med. 2014 Jun;40(6):924. Hoorn, Ewout [corrected to Hoorn, Ewout J]]. Intensive Care Med. 2014;40(3):320-331. doi:10.1007/s00134-014-3210-2
4.Spasovski G, Vanholder R, Allolio B, et al. Clinical practice guideline on diagnosis and treatment of hyponatraemia [published correction appears in Eur J Endocrinol. 2014 Jul;171(1):X1]. Eur J Endocrinol. 2014;170(3):G1-G47. Published 2014 Feb 25. doi:10.1530/EJE-13-1020
5.Spasovski G, Vanholder R, Allolio B, et al. Clinical practice guideline on diagnosis and treatment of hyponatraemia [published correction appears in Nephrol Dial Transplant. 2014 Jun;40(6):924]. Nephrol Dial Transplant. 2014;29 Suppl 2:i1-i39. doi:10.1093/ndt/gfu040
6.Hoorn EJ, Halperin ML, Zietse R. Diagnostic approach to a patient with hyponatraemia: traditional versus physiology-based options. QJM. 2005;98(7):529-540. doi:10.1093/qjmed/hci081
7.Fenske W, Maier SK, Blechschmidt A, Allolio B, Störk S. Utility and limitations of the traditional diagnostic approach to hyponatremia: a diagnostic study [published correction appears in Am J Med. 2011 Oct;124(10):e9]. Am J Med. 2010;123(7):652-657. doi:10.1016/j.amjmed.2010.01.013
8.Kadiyala R, Kamath C, Baglioni P, Geen J, Okosieme OE. Can a random serum cortisol reduce the need for short synacthen tests in acute medical admissions?. Ann Clin Biochem. 2010;47(Pt 4):378-380. doi:10.1258/acb.2010.010008
9.Kilpatrick ES. Disorders of sodium balance: hypothyroidism and hyponatraemia: an old wives' tale?. BMJ. 2006;332(7545):854. doi:10.1136/bmj.332.7545.854
10.Pantalone KM, Hatipoglu BA. Hyponatremia and the Thyroid: Causality or Association?. J Clin Med. 2014;4(1):32-36. Published 2014 Dec 26. doi:10.3390/jcm4010032
11.Alessandro P et al.(2021) Disorders of Fluid and Electrolyte Metabolism Docus on Hyponatoremia. Verbalis, Josephh G.(柴垣有吾 監修 冨永直人 槙村益久 志水英明 監訳 (2021) 低Na血症 中外医学社)
12.Ewout J Hoorn, MD, PhDRichard H Sterns, MD. Causes of hyponatremia without hypotonicity (including pseudohyponatremia). In: UpToDate, Post TW (Ed), UpToDate, Waltham, MA. (Accessed on February 28, 2022.)
13.藤田芳郎ら(2015) 研修医のための輸液 水電解質 酸塩基平衡 中外医学社
14.Singh TD, Fugate JE, Rabinstein AA. Central pontine and extrapontine myelinolysis: a systematic review. Eur J Neurol. 2014;21(12):1443-1450. doi:10.1111/ene.12571
15.植西 憲達. 低ナトリウム血症. INTENSIVIST 7;477-492 (2015) 3)
16.Louis G, et al: Long-term outcome of patients hospitalised in intensive care units with central or extrapontine myelinolysis. Crit Care Med 2012; 40: 970-972.
17.Baek SH, Jo YH, Ahn S, et al. Risk of Overcorrection in Rapid Intermittent Bolus vs Slow Continuous Infusion Therapies of Hypertonic Saline for Patients With Symptomatic Hyponatremia: The SALSA Randomized Clinical Trial. JAMA Intern Med. 2021;181(1):81-92. doi:10.1001/jamainternmed.2020.5519
18.Adrogué HJ, Madias NE. Hyponatremia. N Engl J Med. 2000;342(21):1581-1589. doi:10.1056/NEJM200005253422107
19.Berl T. The Adrogue-Madias formula revisited. Clin J Am Soc Nephrol. 2007;2(6):1098-1099. doi:10.2215/CJN.03300807
20.Sood L, Sterns RH, Hix JK, Silver SM, Chen L. Hypertonic saline and desmopressin: a simple strategy for safe correction of severe hyponatremia. Am J Kidney Dis. 2013;61(4):571-578. doi:10.1053/j.ajkd.2012.11.032
21.Atsariyasing W, Goldman MB. A systematic review of the ability of urine concentration to distinguish antipsychotic- from psychosis-induced hyponatremia. Psychiatry Res. 2014;217(3):129-133. doi:10.1016/j.psychres.2014.03.021
以下のアンケートにもご回答いただけますと幸いです。よろしくお願いいたします。